
Microscopia ottica avanzata

Panoramica
La microscopia ottica è una tecnica potente che consente agli scienziati di ingrandire e studiare strutture minuscole, invisibili a occhio nudo, come cellule e molecole.
Utilizzando luce visibile e lenti specializzate, i ricercatori possono osservare in tempo reale i dettagli più intricati dei campioni biologici.
Presso IFOM, l’Unità di Advanced Light Microscopy mette a disposizione tecnologie di imaging all’avanguardia, che permettono di esplorare il mondo microscopico con un livello di dettaglio senza precedenti. Offriamo tecniche di microscopia ad alta e super-risoluzione, che superano i limiti della microscopia ottica convenzionale.
Questi metodi avanzati consentono di visualizzare strutture fino alla scala dei nanometri, contribuendo a svelare processi chiave della biologia cellulare, della ricerca sul cancro e oltre.
Il nostro team di esperti supporta gli scienziati in ogni fase, dalla preparazione e acquisizione dei campioni fino all’analisi dei dati complessi.
Nel corso degli anni, abbiamo costruito una facility all’avanguardia specificamente pensata per promuovere la ricerca sul cancro.
Combinando tecnologie di imaging sofisticate con competenze specialistiche, miriamo a comprendere meglio il cancro su diversi livelli - dalle singole molecole ai tessuti - contribuendo così a nuove scoperte e potenziali trattamenti.
Tecniche di microscopia avanzata
Per migliorare la nostra comprensione della biologia del cancro a diverse scale, ci siamo impegnati nell’ottimizzazione e nell’ampliamento dell’accesso a una vasta gamma di tecniche di microscopia ottica, tra cui:
- Mobilità molecolare:
Optogenetica, Fotoattivazione/photoswitching, FLIP (Fluorescence Loss in Photobleaching), FRAP (Fluorescence Recovery After Photobleaching) - Microiniezione/Micromanipolazione
- Microscopia non lineare:
Eccitazione a due fotoni (2PE), Generazione di seconda armonica (SHG) - Interazioni proteiche:
Colocalizzazione, FRET (Fluorescence Resonance Energy Transfer), Imaging basato sul tempo di vita della fluorescenza - Stimolazione laser-indotta:
Risposta al danno indotto al DNA, Ablazione laser - Meccanobiologia
- Nanoscopia:
Microscopia a super-risoluzione (STED) - Microscopia correlative luce-elettroni (CLEM)
Supporto alla preparazione dei campioni
Forniamo assistenza per la preparazione e la colorazione dei campioni, sia per esperimenti su cellule vive che su cellule fissate. In particolare, offriamo:
- Protocolli per immunofluorescenza e colorazione di cellule vive.
- Protocolli per la chiarificazione di organoidi e tessuti
- Fornitura di reagenti (anticorpi di uso comune, DAPI per la colorazione dei nuclei, anticorpi coniugati per la microscopia STED)
- Supporto per ottimizzare la preparazione e l’acquisizione dei campioni
Analisi delle immagini ed elaborazione dati
Con circa 180 protocolli di analisi personalizzati sviluppati annualmente, il nostro team fornisce supporto immediatamente dopo la raccolta dei dati, dall’elaborazione delle immagini, alla loro analisi e interpretazione. Tutti i plugin e le pippelines possono essere sviluppati in software open-source (Fiji, CellProfiler, QuPath) o su piattaforme commerciali (Matlab, Arivis, Harmony, Prism).
Esempi di strumenti implementati includono:
- Rilevamento di cellule, nuclei e particelle:
Segmentazione e classificazione con metodi classici e/o machine learning (2D e 3D) - Tracking di cellule e particelle:
Pipeline per il tracking cellulare, PIV (Particle Image Velocimetry), wound healing e traffico di particelle - Motilità molecolare:
Analisi di FRAP - Analisi di imaging label-free:
Analisi dell’orientamento delle fibre di collagene con strumenti di machine learning - Interazioni proteiche:
Quantificazione della colocalizzazione, formazione di foci (2D e 3D), analisi FRET - Analisi di immagini di immunoistochimica:
Pipeline di rilevamento oggetti con segmentazione con soglia di colore o machine learning (modelli pre-addestrati o personalizzati), applicabile ad analisi di vetrini interi o singole immagini - Analisi immagini assistita da IA
Integrazione di strumenti di intelligenza artificiale e machine learning per migliorare segmentazione, tracking e analisi quantitativa
Formazione e supporto
Offriamo supporto completo e personalizzato sia per ricercatori senior che per scienziati all’inizio della carriera, favorendo lo sviluppo delle competenze necessarie per sfruttare al meglio le risorse avanzate di microscopia disponibili presso IFOM.
Microscopi disponibili
- Microscopi a campo largo(4 upright, 1 invertito, 1 stereoscopico) per microscopia in fluorescenza e/o a luce trasmessa
- IXplore (Evident): Microscopio a campo largo per imaging di cellule vive o campioni fissati
- Thunder (Leica): Microscopio a campo largo con deconvoluzione computazionale per l’imaging di cellule vive o campioni fissati
- DeltaVision (GE Healthcare):Microscopio a campo largo con deconvoluzione per campioni fissati o imaging di cellule vive
- TIRFM(Leica): microscopio a riflessione interna totale, per l’imaging di cellule vive o campioni fissati
- Spinning Disk CSU (Evident): Microscopia a campo largo, confocale a spinning disk e fotomanipolazione per l’imaging di cellule vive o campioni fissati
- TCS SP2 AOBS (Leica): Microscopio confocale
- TCS SP5 Inverted (Leica): Microscopia confocale, non lineare e fotomanipolazione per campioni fissati o cellule vive
- TCS SP5 Upright (Leica): Microscopia confocale, non lineare, per campioni fissati o cellule vive; imaging intravitale
- TCS SP8 STED (Leica): Microscopia confocale, a super risoluzione (STED), FLIM (Fluorescence Lifetime Imaging Microscopy), fotomanipolazione, per campioni fissati o cellule vive
- TCS SP8 DLS (Leica): Microscopia confocale e Light Sheet per campioni fissati o cellule vive
- Stellaris 8 DIVE (Leica): Microscopia confocale, non lineare, FLIM, fotomanipolazione, per campioni fissati o cellule vive; imaging intravitale
Maggiori informazioni
Altra strumentazione
- Envision (Revvity): Lettore di micropiastre
- AIS2: Sistema di microiniezione
- CellASIC ONIX2 (Merck): Sistema microfluidico
Ringraziamenti alla Facility
In base alle Core Facilities Guidelines, qualora i servizi di una Facility siano stati utilizzati in un lavoro descritto in una pubblicazione, la Facility deve essere citata nei ringraziamenti, indicando sia il nome della Facility sia il relativo Research Resource Identifier (RRID).
Esempio di ringraziamento:
Il lavoro descritto è stato supportato dalla IFOM Microscopia Ottica Avanzata Core Facility (RRID: SCR_026866).
Co‑Authorship
Se un membro dello staff di una Core Facility IFOM o Cogentech contribuisce in modo sostanziale a un lavoro pubblicato, deve essere incluso come co‑autore.
Ulteriori informazioni sono disponibili nelle sezioni Recommended guidelines e Acknowledging and citing core facilities
Esempi di contributi sostanziali che possono giustificare la co‑autorship includono:
- Contributo alla progettazione sperimentale o all’ottimizzazione degli esperimenti
- Sviluppo o adattamento significativo di metodi o protocolli
- Analisi avanzata e interpretazione dei dati
- Contributo intellettuale che ha influenzato la direzione scientifica dello studio
Il supporto tecnico di routine o l’erogazione di servizi standard, di norma, giustificano il solo ringraziamento e non la co‑autorship.
- PMID: 39536107
USP1 deubiquitinates PARP1 to regulate its trapping and PARylation activity.
Nespolo A, Stefenatti L, Pellarin I, Gambelli A, Rampioni Vinciguerra GL, Karimbayli J, Barozzi S, Orsenigo F, Spizzo R, Nicoloso MS, Segatto I, D'Andrea S, Bartoletti M, Lucia E, Giorda G, Canzonieri V, Puglisi F, Belletti B, Schiappacassi M, Baldassarre G, Sonego M.
2024 Jan 2;84(1):133-153. doi: 10.1158/0008-5472.CAN-23-1129. PMID: 37855660 Free PMC article. - PMID: 39218980
Emerin mislocalization during chromatin bridge resolution can drive prostate cancer cell invasiveness in a collagen-rich microenvironment.
Popęda M, Kowalski K, Wenta T, Beznoussenko GV, Rychłowski M, Mironov A, Lavagnino Z, Barozzi S, Richert J, Bertolio R, Myszczyński K, Szade J, Bieńkowski M, Miszewski K, Matuszewski M, Żaczek AJ, Braga L, Del Sal G, Bednarz-Knoll N, Maiuri P, Nastały P.
Exp Mol Med. 2024 Sep;56(9):2016-2032. doi: 10.1038/s12276-024-01308-w. Epub 2024 Sep 2. PMID: 39218980 Free PMC article. - PMID: 39155303
CDK12 controls transcription at damaged genes and prevents MYC-induced transcription-replication conflicts.
Curti L, Rohban S, Bianchi N, Croci O, Andronache A, Barozzi S, Mattioli M, Ricci F, Pastori E, Sberna S, Bellotti S, Accialini A, Ballarino R, Crosetto N, Wade M, Parazzoli D, Campaner S.
Nat Commun. 2024 Aug 18;15(1):7100. doi: 10.1038/s41467-024-51229-5.PMID: 39155303 Free PMC article. - PMID: 39208097
A p62-dependent rheostat dictates micronuclei catastrophe and chromosome rearrangements.
Martin S, Scorzoni S, Cordone S, Mazzagatti A, Beznoussenko GV, Gunn AL, Di Bona M, Eliezer Y, Leor G, Ben-Yishay T, Loffreda A, Cancila V, Rainone MC, Ippolito MR, Martis V, Bedin F, Garrè M, Vaites LP, Vasapolli P, Polo S, Parazzoli D, Tripodo C, Mironov AA, Cuomo A, Ben-David U, Bakhoum SF, Hatch EM, Ly P, Santaguida S.
Science. 2024 Aug 30;385(6712):eadj7446. doi: 10.1126/science.adj7446. Epub 2024 Aug 30.PMID: 39208097 Free PMC article. - PMID: 38977673
Mechanically induced topological transition of spectrin regulates its distribution in the mammalian cell cortex.
Ghisleni A, Bonilla-Quintana M, Crestani M, Lavagnino Z, Galli C, Rangamani P, Gauthier NC.
Nat Commun. 2024 Jul 8;15(1):5711. doi: 10.1038/s41467-024-49906-6.PMID: 38977673 Free PMC article. - PMID: 38990945
Mechanical stress during confined migration causes aberrant mitoses and c-MYC amplification.
Bastianello G, Kidiyoor GR, Lowndes C, Li Q, Bonnal R, Godwin J, Iannelli F, Drufuca L, Bason R, Orsenigo F, Parazzoli D, Pavani M, Cancila V, Piccolo S, Scita G, Ciliberto A, Tripodo C, Pagani M, Foiani M.
Proc Natl Acad Sci U S A. 2024 Jul 16;121(29):e2404551121. doi: 10.1073/pnas.2404551121. Epub 2024 Jul 11.PMID: 38990945 Free PMC article. - PMID: 39087467
GPR126 is a specifier of blood-brain barrier formation in the mouse central nervous system.
Kakogiannos N, Scalise AA, Martini E, Maderna C, Benvenuto AF, D'Antonio M, Carmignani L, Magni S, Gullotta GS, Lampugnani MG, Iannelli F, Beznoussenko GV, Mironov AA, Cerutti C, Bentley K, Philippides A, Zanardi F, Bacigaluppi M, Sigismund S, Bassani C, Farina C, Martino G, De Giovanni M, Dejana E, Iannacone M, Inverso D, Giannotta M.
J Clin Invest. 2024 Jun 6;134(15):e165368. doi: 10.1172/JCI165368.PMID: 39087467 Free PMC article. -
PMID: 38088930
Cell stretching activates an ATM mechano-transduction pathway that remodels cytoskeleton and chromatin.
Bastianello G, Porcella G, Beznoussenko GV, Kidiyoor G, Ascione F, Li Q, Cattaneo A, Matafora V, Disanza A, Quarto M, Mironov AA, Oldani A, Barozzi S, Bachi A, Costanzo V, Scita G, Foiani M.
Cell Rep. 2023 Dec 26;42(12):113555. doi: 10.1016/j.celrep.2023.113555. Epub 2023 Dec 11.PMID: 38088930 Free PMC article. -
PMID: 37925537
Alternative lengthening of telomeres (ALT) cells viability is dependent on C-rich telomeric RNAs.
Rosso I, Jones-Weinert C, Rossiello F, Cabrini M, Brambillasca S, Munoz-Sagredo L, Lavagnino Z, Martini E, Tedone E, Garre' M, Aguado J, Parazzoli D, Mione M, Shay JW, Mercurio C, d'Adda di Fagagna F.
Nat Commun. 2023 Nov 4;14(1):7086. doi: 10.1038/s41467-023-42831-0. PMID: 37925537 Free PMC article. -
PMID: 37713487
Clonal cooperation through soluble metabolite exchange facilitates metastatic outgrowth by modulating Allee effect.
Hershey BJ, Barozzi S, Orsenigo F, Pompei S, Iannelli F, Kamrad S, Matafora V, Pisati F, Calabrese L, Fragale G, Salvadori G, Martini E, Totaro MG, Magni S, Guan R, Parazzoli D, Maiuri P, Bachi A, Patil KR, Cosentino Lagomarsino M, Havas KM.
Sci Adv. 2023 Sep 15;9(37):eadh4184. doi: 10.1126/sciadv.adh4184. Epub 2023 Sep 15. PMID: 37713487 Free PMC article. -
PMID: 36581770
Tissue fluidification promotes a cGAS-STING cytosolic DNA response in invasive breast cancer.
Frittoli E, Palamidessi A, Iannelli F, Zanardi F, Villa S, Barzaghi L, Abdo H, Cancila V, Beznoussenko GV, Della Chiara G, Pagani M, Malinverno C, Bhattacharya D, Pisati F, Yu W, Galimberti V, Bonizzi G, Martini E, Mironov AA, Gioia U, Ascione F, Li Q, Havas K, Magni S, Lavagnino Z, Pennacchio FA, Maiuri P, Caponi S, Mattarelli M, Martino S, d'Adda di Fagagna F, Rossi C, Lucioni M, Tancredi R, Pedrazzoli P, Vecchione A, Petrini C, Ferrari F, Lanzuolo C, Bertalot G, Nader G, Foiani M, Piel M, Cerbino R, Giavazzi F, Tripodo C, Scita G.
Nat Mater. 2023 May;22(5):644-655. doi: 10.1038/s41563-022-01431-x. Epub 2022 Dec 29.PMID: 36581770 Free PMC article. -
PMID: 36894671
SARS-CoV-2 infection induces DNA damage, through CHK1 degradation and impaired 53BP1 recruitment, and cellular senescence.
Gioia U, Tavella S, Martínez-Orellana P, Cicio G, Colliva A, Ceccon M, Cabrini M, Henriques AC, Fumagalli V, Paldino A, Presot E, Rajasekharan S, Iacomino N, Pisati F, Matti V, Sepe S, Conte MI, Barozzi S, Lavagnino Z, Carletti T, Volpe MC, Cavalcante P, Iannacone M, Rampazzo C, Bussani R, Tripodo C, Zacchigna S, Marcello A, d'Adda di Fagagna F.
Nat Cell Biol. 2023 Apr;25(4):550-564. doi: 10.1038/s41556-023-01096-x. Epub 2023 Mar 9.PMID: 36894671 Free PMC article. -
PMID: 36460033
Decellularized extracellular matrix as scaffold for cancer organoid cultures of colorectal peritoneal metastases.
Varinelli L, Guaglio M, Brich S, Zanutto S, Belfiore A, Zanardi F, Iannelli F, Oldani A, Costa E, Chighizola M, Lorenc E, Minardi SP, Fortuzzi S, Filugelli M, Garzone G, Pisati F, Vecchi M, Pruneri G, Kusamura S, Baratti D, Cattaneo L, Parazzoli D, Podestà A, Milione M, Deraco M, Pierotti MA, Gariboldi M.
J Mol Cell Biol. 2023 Apr 6;14(11):mjac064. doi: 10.1093/jmcb/mjac064. PMID: 36460033 Free PMC article.
Strumentazione
Gallery
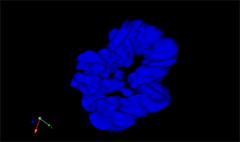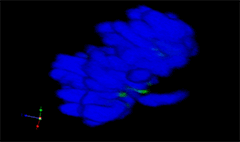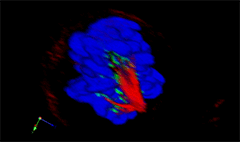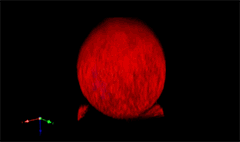
3D rendering of a mitotic He-La cell
(blue chromatin, green CREST, red tubulin)
Strumentazione
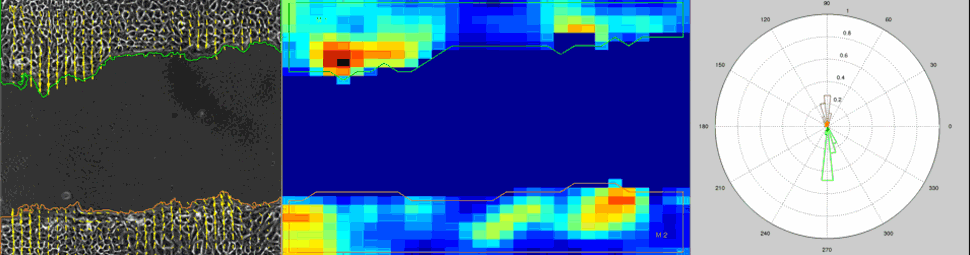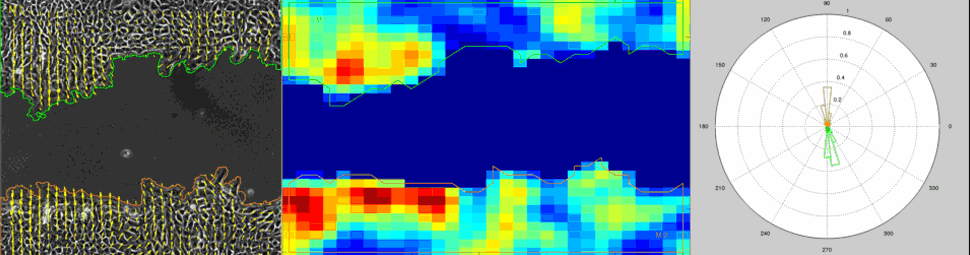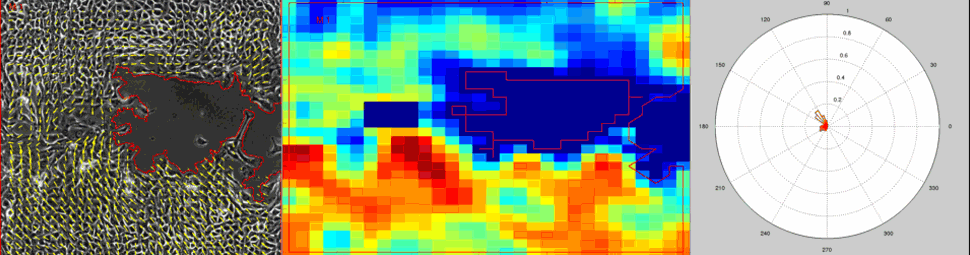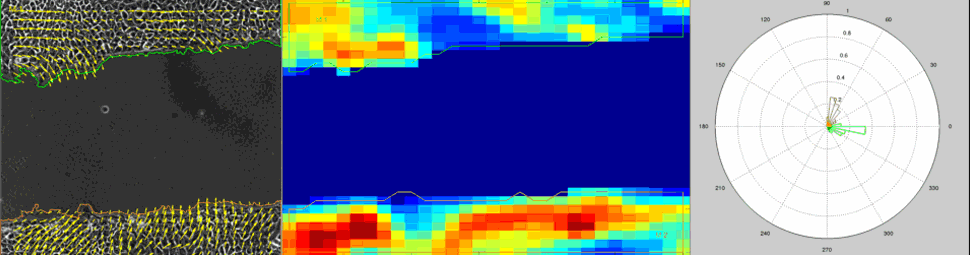
Particle Image Velocimetry (PIV) Analysis of a wound healing experiment

Dario Parazzoli
Dario Parazzoli coltiva da sempre la passione per l’intersezione tra fisica e biologia. Dopo la laurea in Fisica all’Università di Milano, dove ha studiato la dispersione di radionuclidi a seguito del disastro di Chernobyl, ha iniziato la sua carriera nell’industria della microscopia. Per quasi un decennio ha lavorato come project manager, contribuendo allo sviluppo della microscopia confocale e di soluzioni di imaging di fascia alta per le scienze della vita.
Nel 2004 è passato alla ricerca biomedica presso l’Istituto Europeo di Oncologia, dove ha adattato la microscopia TIRF (Total Internal Reflection Fluorescence) per imaging live a lungo termine. Ha poi fondato una facility di imaging presso l’Istituto Nazionale di Genetica Molecolare, prima di approdare a IFOM nel 2009.
Oggi, come responsabile dell’Unità di Advanced Light Microscopy, Dario supervisiona tecnologie di imaging all’avanguardia a supporto della ricerca sul cancro, promuovendo l’innovazione nella microscopia biomedica e contribuendo alla comprensione dei processi cellulari.






















