Screening Genomico Funzionale

Panoramica
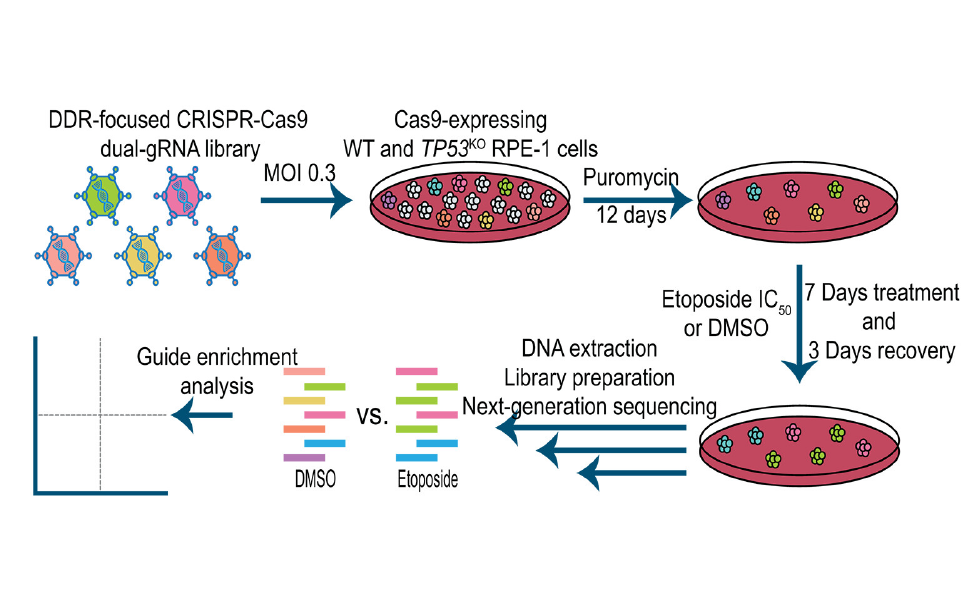
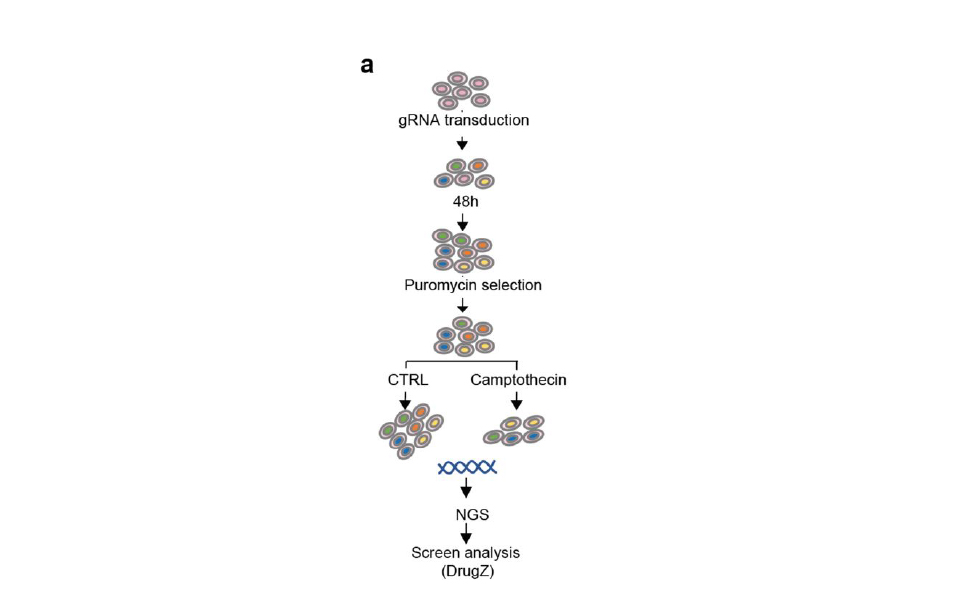
CRISPR/Cas9 è uno strumento rivoluzionario di editing genomico, derivato dai meccanismi di difesa naturali dei batteri. Quando infettati, i batteri incorporano segmenti di DNA virale nelle loro sequenze CRISPR (Clustered Regularly Interspaced Short Palindromic Repeats). In caso di un nuovo attacco virale, l'enzima Cas9 (CRISPR-associated protein 9) utilizza le molecole di RNA trascritte dalle sequenze CRISPR per riconoscere il DNA virale e neutralizzare il virus. Nel 2012, le vincitrici del Premio Nobel per la Chimica Jennifer Doudna ed Emmanuelle Charpentier hanno adattato questo sistema alle cellule eucariotiche, creando uno strumento di editing genomico che taglia il DNA e sfrutta i meccanismi di riparazione cellulare per introdurre modifiche genetiche. L'Unità di Screening di Genomica Funzionale (FGS) conduce screening CRISPR su larga scala utilizzando librerie pooled o arrayed in vari modelli cellulari. Questa tecnologia consente di valutare gli effetti di migliaia di perturbazioni genetiche a livello della singola cellula attraverso approcci di CRISPR knockout (CRISPR KO), CRISPR interference (CRISPRi) e CRISPR activation (CRISPRa). Tale sistema utilizza inoltre base o prime editing per ricapitolare mutazioni specifiche, come quelle rilevanti per lo sviluppo e la progressione del cancro. Il base editing combina un modulo Cas con una deaminasi per convertire le basi del DNA, mentre il prime editing utilizza un templato di RNA per introdurre modifiche genetiche mirate nel DNA target. L'Unità FGS integra queste perturbazioni con vari readouts, tra cui vitalità cellulare e analisi fenotipiche complesse, spesso in collaborazione con Imaging, FACS Facility ed ETP. L'analisi dei dati è supportata dall'Unità di Bioinformatica IFOM. Collaborando con diversi gruppi IFOM, l'Unità FGS mira a chiarire le funzioni dei singoli geni, comprendere i loro ruoli nei meccanismi delle malattie, e ad identificare nuovi bersagli terapeutici. Oltre a supportare i ricercatori dell'IFOM sviluppando e ottimizzando strumenti basati su CRISPR/Cas, l'Unità adotta tali tecnologie per investigare la risposta al danno del DNA su larga scala.
La struttura di screening genomico funzionale offre screening completi e ad alta produttività basati su CRISPR su misura per la ricerca sul cancro, tra cui screening CRISPR knockout (KO), interferenza (CRISPRi), attivazione (CRISPRa) e modifica delle basi per valutare sistematicamente la funzione genica in modelli in vitro e in vivo. In particolare, la struttura offre:
- Sviluppo di test personalizzati, compresa la definizione delle migliori condizioni sperimentali per lo screening
- Progettazione della libreria
- Amplificazione della libreria, confezionamento del virus e ottimizzazione delle condizioni di trasduzione
- Ottimizzazione dei risultati funzionali dello screening (in collaborazione con la struttura di citometria a flusso per gli screening basati su FACS)
- Esecuzione dello screening, estrazione del DNA genomico e preparazione dei campioni NGS
- Analisi e interpretazione dei dati in collaborazione con il dipartimento Research Data & Biocomputing Science dell'IFOM, garantendo un'analisi e un'interpretazione rigorosa dei dati.
Collaborazioni
PI collaboratori nell'ambito di Athena, il piano strategico dell'IFOM:
4D-Nucleofector® X Unit
Ringraziamenti alla Facility
In base alle Core Facilities Guidelines, qualora i servizi di una Facility siano stati utilizzati in un lavoro descritto in una pubblicazione, la Facility deve essere citata nei ringraziamenti, indicando sia il nome della Facility sia il relativo Research Resource Identifier (RRID).
Esempio di ringraziamento:
Il lavoro descritto è stato supportato dalla IFOM Screening Genomico Funzionale Core Facility (RRID: SCR_026867).
Co‑Authorship
Se un membro dello staff di una Core Facility IFOM o Cogentech contribuisce in modo sostanziale a un lavoro pubblicato, deve essere incluso come co‑autore.
Ulteriori informazioni sono disponibili nelle sezioni Recommended guidelines e Acknowledging and citing core facilities
Esempi di contributi sostanziali che possono giustificare la co‑autorship includono:
- Contributo alla progettazione sperimentale o all’ottimizzazione degli esperimenti
- Sviluppo o adattamento significativo di metodi o protocolli
- Analisi avanzata e interpretazione dei dati
- Contributo intellettuale che ha influenzato la direzione scientifica dello studio
Il supporto tecnico di routine o l’erogazione di servizi standard, di norma, giustificano il solo ringraziamento e non la co‑autorship.
- Decitabine cytotoxicity is promoted by dCMP deaminase DCTD and mitigated by SUMO-dependent E3 ligase TOPORS CJ Carnie, MJ Gotz, CS Palma-Chaundler, P Weickert, A Wanders, ... The EMBO Journal, 1-27 (2024)
- Transcription-coupled repair of DNA–protein cross-links depends on CSA and CSB CJ Carnie, AC Acampora, AS Bader, C Erdenebat, S Zhao, E Bitensky, ... Nature Cell Biology, 1-14 (2024)
- Cockayne syndrome proteins CSA and CSB promote transcription-coupled repair of DNA-protein crosslinks independently of nucleotide excision repair C Carnie, A Acampora, A Bader, V Gupta, G D'Alessandro, ... Nature Research (2024)
- USP37 prevents premature disassembly of stressed replisomes by TRAIP OV Kochenova, G D'Alessandro, D Pilger, E Schmid, SL Richards, ... bioRxiv, 2024.09.03.611025 (2024)
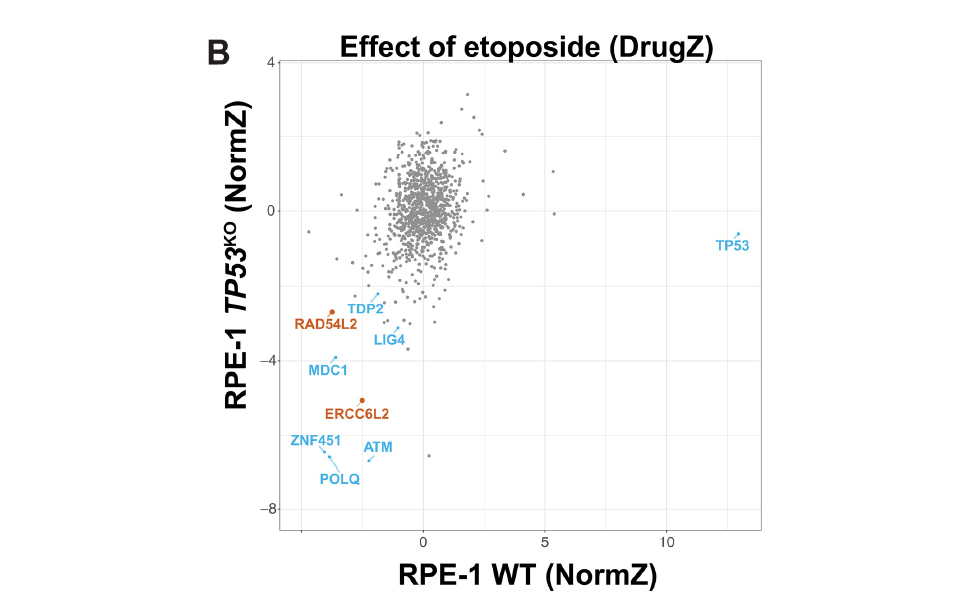
- RAD54L2 counters TOP2-DNA adducts to promote genome stability G D’Alessandro, DA Morales-Juarez, SL Richards, KC Nitiss, ... Science Advances 9 (49), eadl2108 (2023)
- The dCMP deaminase DCTD and the E3 ligase TOPORS are central mediators of decitabine cytotoxicity CJ Carnie, MJ Gotz, CS Palma-Chaundler, P Weickert, AR Wanders, ... bioRxiv, 2023.12.21.572728 (2023)
- BRCA2 controls DNA: RNA hybrid level at DSBs by mediating RNase H2 recruitment G D’Alessandro, DR Whelan, SM Howard, V Vitelli, X Renaudin, ... Nature Communications 9 (1), 5376 (2018)
- THE ROLE OF RNA AND DNA: RNA HYBRIDS AT DNA DOUBLE-STRAND BREAKS G D'Alessandro Università degli Studi di Milano (2018)
- Long non-coding RNA in the control of genome stability and cancer phenotypes G D’Alessandro, FA di Fagagna Non-coding RNA Investigation 2 (3) (2018)
- A role for RNA and DNA: RNA hybrids in the modulation of DNA repair by homologous recombination G D’Alessandro, M Adamowicz, D Whelan, SM Howard, ... bioRxiv, 255976 (2018)
- Transcription and DNA damage: holding hands or crossing swords? G D'Alessandro, FA di Fagagna Journal of Molecular Biology 429 (21), 3215-3229 (2017)
- A damaged genome’s transcriptional landscape through multilayered expression profiling around in situ-mapped DNA double-strand breaks F Iannelli, A Galbiati, I Capozzo, Q Nguyen, B Magnuson, F Michelini, ... Nature Communications 8 (1), 15656 (2017)
- Rearrangements of chromosome bands 15q12-q21 are secondary to HMGA2 deregulation in conventional lipoma G Macchia, KH Nord, G D'Alessandro, J Nilsson, L Magnusson, ... Oncology Reports 31 (2), 807-811 (2014)
- NEW FUSION GENE INVOLVING EWSR1 IN ACUTE MYELOID LEUKEMIA G Macchia, G D'Alessandro, C Lo Cunsolo, M Carella, O Palumbo, ... HAEMATOLOGICA 97 (s2), S133-S133 (2012)
Gallery

Giuseppina D’Alessandro
Giuseppina D'Alessandro ha conseguito la laurea in Biotecnologie Mediche presso l'Università di Bari e il dottorato di ricerca in Medicina Molecolare presso l'IFOM di Milano. Il suo lavoro di dottorato, svolto nel laboratorio del Dr. d'Adda di Fagagna, si è concentrato sul ruolo dell'RNA e degli ibridi DNA:RNA nella riparazione delle rotture a doppio filamento del DNA.
Successivamente è entrata a far parte dell'Università di Cambridge come Marie Skłodowska-Curie iCARE-2 Fellow, lavorando nel laboratorio del Prof. Sir Steve Jackson.
Durante la sua formazione post-dottorato presso il Gurdon Institute e il Cancer Research UK Cambridge Institute, si è specializzata nell'editing genomico e nella risposta al danno al DNA, utilizzando tecnologie CRISPR avanzate, tra cui approcci di knock-out, inibizione e editing delle basi.
Dopo cinque anni nel Regno Unito, Giuseppina è tornata in Italia per fondare e dirigere il Functional Genomics Screening Core Facility presso l'IFOM. In questo ruolo, applica la sua esperienza nell'editing genomico e nello screening per supportare i ricercatori dell'IFOM ed esplorare i meccanismi di riparazione del DNA su larga scala.
Giuseppina ha guidato diversi progetti di ricerca e coordinato collaborazioni internazionali.
È anche revisore per riviste internazionali, tra cui Nature Communications, e contribuisce al servizio di preprint highlights PreLights.