Microscopia elettronica cellulare e dei tessuti

Panoramica
La microscopia elettronica (EM) è uno strumento potente nella ricerca sul cancro, che offre una risoluzione senza pari per osservare strutture che rimangono invisibili ai microscopi ottici tradizionali. Comprendere il cancro a livello ultrastrutturale è essenziale per studiare lo sviluppo dei tumori, la progressione della malattia e gli effetti dei potenziali trattamenti.
Presso l'IFOM, la nostra struttura centrale di microscopia elettronica per cellule e tessuti fornisce competenze nel campo della microscopia elettronica per analizzare un'ampia gamma di campioni biologici, dalle cellule coltivate ai tessuti. L'EM consente ai ricercatori di studiare i dettagli più fini degli organelli e dei compartimenti subcellulari, contribuendo a scoprire come gli oncogeni influenzano l'organizzazione e la funzione cellulare. Ad esempio, la microscopia elettronica consente lo studio degli esosomi e del loro ruolo nella tumorigenesi, nonché l'individuazione di alterazioni morfologiche indotte dal knockdown o dal knockout genico, cambiamenti che altrimenti passerebbero inosservati.
La nostra struttura offre una gamma completa di metodi avanzati, tra cui immuno-EM, microscopia ottica-elettronica correlativa (CLEM), EM tridimensionale (3DEM) e analisi ultrastrutturale quantitativa. Sviluppando tecniche innovative come il video CLEM per organelli dinamici e nuovi metodi di preparazione dei campioni per 3DEM, perfezioniamo continuamente il nostro approccio per soddisfare le esigenze in continua evoluzione dei ricercatori sul cancro.
La struttura centrale di microscopia elettronica per cellule e tessuti dell'IFOM fornisce un'ampia gamma di tecniche di imaging avanzate a supporto della ricerca nella biologia del cancro e nell'ultrastruttura cellulare.
Tecniche attuali
- Microscopia elettronica a trasmissione (TEM) – Imaging ad alta risoluzione di strutture cellulari e subcellulari.
- vMicroscopia elettronica a trasmissione a scansione (STEM) – Combina la risoluzione TEM con capacità di scansione per analisi approfondite.
- Immuno-microscopia elettronica (Immuno-EM) – Consente la localizzazione di proteine specifiche all'interno delle cellule utilizzando la marcatura con nanoparticelle d'oro.
- Microscopia ottica ed elettronica correlativa (CLEM) – Unisce la microscopia a fluorescenza con la microscopia elettronica per collegare i dati molecolari e ultrastrutturali.
- Microscopia elettronica tridimensionale (3DEM) – Fornisce ricostruzioni 3D dettagliate delle strutture cellulari.
Metodi innovativi e direzioni future
Sviluppiamo e perfezioniamo continuamente metodologie per migliorare le applicazioni EM, tra cui:
- Video-CLEM, ideale per lo studio di organelli in rapido movimento.
- Rotatore discretizzato, uno strumento stereologico per una quantificazione strutturale precisa.
- Nuove tecniche di preparazione dei campioni per 3DEM, che ottimizzano la risoluzione e l'accuratezza dei dati.
Guardando al futuro, miriamo a:
- Migliorare le metodologie CLEM e 3DEM per una maggiore precisione.
- Sviluppare nuovi approcci di analisi quantitativa utilizzando stimatori stereologici assoluti.
- Progettare protocolli personalizzati di preparazione dei campioni per soddisfare le esigenze di ricerca specifiche degli scienziati IFOM.
Il nostro obiettivo finale è quello di stabilire linee guida moderne per le applicazioni della microscopia elettronica in oncologia, garantendo ai ricercatori l'accesso alle soluzioni di imaging più avanzate e affidabili.
Collaborazioni
La struttura collabora con gli scienziati dell'IFOM nell'ambito del piano strategico Athena:
- Microscopio elettronico a trasmissione Tecnai G2 20 Twin - FEI Italia Srl (ora Thermo Fisher Scientific). Imaging (S)TEM ad alta qualità e alta risoluzione e tomografia elettronica.
- Leica EM HPM100 è un sistema di congelamento ad alta pressione per la vetrificazione di campioni con spessore fino a 200 μm. Congelatore ad alta pressione per la criofissazione di campioni biologici e industriali.
- Leica EM AFS2 esegue tecniche di sostituzione mediante congelamento e abbassamento progressivo della temperatura (PLT) e consente l'inclusione a bassa temperatura e la polimerizzazione delle resine.
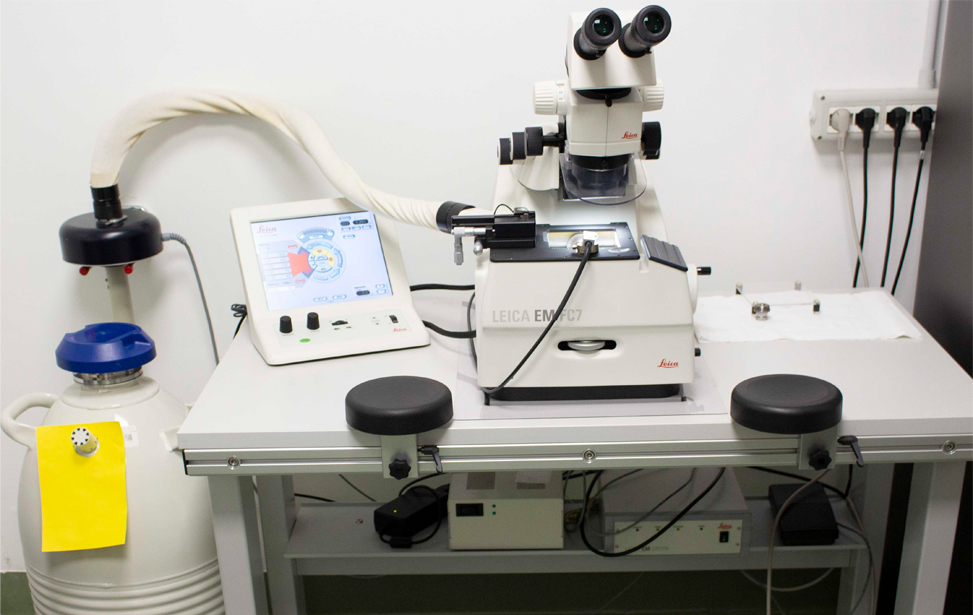
- Leica EM UC7 (a temperatura ambiente) sezioni ultra-sottili o semi-sottili di alta qualità costante a temperatura ambiente
- Leica EM UC7 (CRYO-) La crioultramicrotomia consiste nel tagliare sezioni ultrasottili da un campione congelato. Queste sono abbastanza sottili da poter essere visualizzate in un criomicroscopio a trasmissione (cryo-TEM). Un crioultramicrotomo mantiene temperature inferiori a -140 °C e può tagliare sezioni criogeniche di spessore inferiore a 100 nm.
- Leica EM KMR 3 Il metodo di rottura bilanciata del Leica EM KMR3 garantisce coltelli di vetro perfetti in tre spessori: 6,4 mm, 8 mm e 10 mm.
Ringraziamenti alla Facility
In base alle Core Facilities Guidelines, qualora i servizi di una Facility siano stati utilizzati in un lavoro descritto in una pubblicazione, la Facility deve essere citata nei ringraziamenti, indicando sia il nome della Facility sia il relativo Research Resource Identifier (RRID).
Esempio di ringraziamento:
Il lavoro descritto è stato supportato dalla IFOM Microscopia elettronica cellulare e dei tessuti Core Facility (RRID: SCR_026863).
Co‑Authorship
Se un membro dello staff di una Core Facility IFOM o Cogentech contribuisce in modo sostanziale a un lavoro pubblicato, deve essere incluso come co‑autore.
Ulteriori informazioni sono disponibili nelle sezioni Recommended guidelines e Acknowledging and citing core facilities
Esempi di contributi sostanziali che possono giustificare la co‑autorship includono:
- Contributo alla progettazione sperimentale o all’ottimizzazione degli esperimenti
- Sviluppo o adattamento significativo di metodi o protocolli
- Analisi avanzata e interpretazione dei dati
- Contributo intellettuale che ha influenzato la direzione scientifica dello studio
Il supporto tecnico di routine o l’erogazione di servizi standard, di norma, giustificano il solo ringraziamento e non la co‑autorship.
Key Publications
- Martin S, Scorzoni S, Cordone S, Mazzagatti A, Beznoussenko GV, Gunn AL, Di Bona M, Eliezer Y, Leor G, Ben-Yishay T, Loffreda A, Cancila V, Rainone MC, Ippolito MR, Martis V, Bedin F, Garrè M, Vaites LP, Vasapolli P, Polo S, Parazzoli D, Tripodo C, Mironov AA, Cuomo A, Ben-David U, Bakhoum SF, Hatch EM, Ly P, Santaguida S.
A p62-dependent rheostat dictates micronuclei catastrophe and chromosome rearrangements.
Science. 2024 Aug 30;385(6712): eadj7446. doi: 10.1126/ science. adj 7446. Epub 2024 Aug 30. PMID: 39208097 - Kakogiannos N, Scalise AA, Martini E, Maderna C, Benvenuto AF, D'Antonio M, Carmignani L, Magni S, Gullotta GS, Lampugnani MG, Iannelli F, Beznoussenko GV, Mironov AA, Cerutti C, Bentley K, Philippides A, Zanardi F, Bacigaluppi M, Sigismund S, Bassani C, Farina C, Martino G, De Giovanni M, Dejana E, Iannacone M, Inverso D, Giannotta M.
GPR126 is a specifier of blood-brain barrier formation in the mouse central nervous system.
J Clin Invest. 2024 Jun 6;134(15): e165368. doi: 10.1172/JCI165368. PMID: 39087467. - Popęda M, Kowalski K, Wenta T, Beznoussenko GV, Rychłowski M, Mironov A, Lavagnino Z, Barozzi S, Richert J, Bertolio R, Myszczyński K, Szade J, Bieńkowski M, Miszewski K, Matuszewski M, Żaczek AJ, Braga L, Del Sal G, Bednarz-Knoll N, Maiuri P, Nastały P.
Emerin mislocalization during chromatin bridge resolution can drive prostate cancer cell invasiveness in a collagen-rich microenvironment.
Exp Mol Med. 2024 Sep;56(9):2016-2032. doi: 10.1038/s12276-024-01308-w. Epub 2024 Sep 2. PMID: 39218980 - Bastianello G, Porcella G, Beznoussenko GV, Kidiyoor G, Ascione F, Li Q, Cattaneo A, Matafora V, Disanza A, Quarto M, Mironov AA, Oldani A, Barozzi S, Bachi A, Costanzo V, Scita G, Foiani M.
Cell stretching activates an ATM mechano-transduction pathway that remodels cytoskeleton and chromatin.
Cell Rep. 2023 - Poli A, Pennacchio FA, Ghisleni A, di Gennaro M, Lecacheur M, Nastały P, Crestani M, Pramotton FM, Iannelli F, Beznusenko G, Mironov AA, Panzetta V, Fusco S, Sheth B, Poulikakos D, Ferrari A, Gauthier N, Netti PA, Divecha N, Maiuri P.
PIP4K2B is mechanoresponsive and controls heterochromatin-driven nuclear softening through UHRF1.
Nat Commun. 2023 Mar 14;14(1):1432. doi: 10.1038/s41467-023-37064-0.PMID: 36918565 - Frittoli E, Palamidessi A, Iannelli F, Zanardi F, Villa S, Barzaghi L, Abdo H, Cancila V, Beznoussenko GV, Della Chiara G, Pagani M, Malinverno C, Bhattacharya D, Pisati F, Yu W, Galimberti V, Bonizzi G, Martini E, Mironov AA, Gioia U, Ascione F, Li Q, Havas K, Magni S, Lavagnino Z, Pennacchio FA, Maiuri P, Caponi S, Mattarelli M, Martino S, d'Adda di Fagagna F, Rossi C, Lucioni M, Tancredi R, Pedrazzoli P, Vecchione A, Petrini C, Ferrari F, Lanzuolo C, Bertalot G, Nader G, Foiani M, Piel M, Cerbino R, Giavazzi F, Tripodo C, Scita G.
Tissue fluidification promotes a cGAS-STING cytosolic DNA response in invasive breast cancer.
Nat Mater. 2022 Dec 29. doi: 10.1038/s41563-022-01431-x. PMID: 36581770 - Kidiyoor GR, Li Q, Bastianello G, Bruhn C, Giovannetti I, Mohamood A, Beznoussenko GV, Mironov A, Raab M, Piel M, Restuccia U, Matafora V, Bachi A, Barozzi S, Parazzoli D, Frittoli E, Palamidessi A, Panciera T, Piccolo S, Scita G, Maiuri P, Havas KM, Zhou ZW, Kumar A, Bartek J, Wang ZQ, Foiani M.
ATR is essential for preservation of cell mechanics and nuclear integrity during interstitial migration.
Nat Commun. 2020 Sep 24;11(1):4828. doi: 10.1038/s41467-020-18580-9.PMID: 32973141 - Capaci V, Bascetta L, Fantuz M, Beznoussenko GV, Sommaggio R, Cancila V, Bisso A, Campaner E, Mironov AA, Wiśniewski JR, Ulloa Severino L, Scaini D, Bossi F, Lees J, Alon N, Brunga L, Malkin D, Piazza S, Collavin L, Rosato A, Bicciato S, Tripodo C, Mantovani F, Del Sal G.
Mutant p53 induces Golgi tubulo-vesiculation driving a prometastatic secretome.
Nat Commun. 2020 Aug 7;11(1):3945. doi: 10.1038/s41467-020-17596-5. PMID: 32770028 - Bisi S, Marchesi S, Rizvi A, Carra D, Beznoussenko GV, Ferrara I, Deflorian G, Mironov A, Bertalot G, Pisati F, Oldani A, Cattaneo A, Saberamoli G, Pece S, Viale G, Bachi A, Tripodo C, Scita G, Disanza A.
IRSp53 controls plasma membrane shape and polarized transport at the nascent lumen in epithelial tubules.
Nat Commun. 2020 Jul 14;11(1):3516. doi: 10.1038/s41467-020-17091-x. PMID: 32665580 - Kakogiannos N, Ferrari L, Giampietro C, Scalise AA, Maderna C, Ravà M, Taddei A, Lampugnani MG, Pisati F, Malinverno M, Martini E, Costa I, Lupia M, Cavallaro U, Beznoussenko GV, Mironov AA, Fernandes B, Rudini N, Dejana E, Giannotta M.
JAM-A Acts via C/EBP-α to Promote Claudin-5 Expression and Enhance Endothelial Barrier Function.
Circ Res. 2020 Sep 25;127(8):1056-1073. doi: 10.1161/CIRCRESAHA.120.316742. Epub 2020 Jul 15. PMID: 32673519 - Paulina Nastały, Divya Purushothaman, Stefano Marchesi, Alessandro Poli, Tobias Lendenmann, Gururaj Rao Kidiyoor, Galina V. Beznoussenko, Stefania Lavore, Orso Maria Romano, Dimos Poulikakos, Marco Cosentino Lagomarsino, Alexander A. Mironov, Aldo Ferrari, Paolo Maiuri.
Role of the nuclear membrane protein Emerin in front-rear polarity of the nucleus.
Nat Commun. 2020 May 1;11(1):2122. doi: 10.1038/s41467-020-15910-9.PMID: 32358486 - Palamidessi A, Malinverno C, Frittoli E, Corallino S, Barbieri E, Sigismund S, Beznoussenko GV, Martini E, Garre M, Ferrara I, Tripodo C, Ascione F, Cavalcanti-Adam EA, Li Q, Di Fiore PP, Parazzoli D, Giavazzi F, Cerbino R, Scita G.
Unjamming overcomes kinetic and proliferation arrest in terminally differentiated cells and promotes collective motility of carcinoma.
Nat Mater. 2019 Nov;18(11):1252-1263. - Yang JS, Hsu JW, Park SY, Li J, Oldham WM, Beznoussenko GV, Mironov AA, Loscalzo J, Hsu VW.
GAPDH inhibits intracellular pathways during starvation for cellular energy homeostasis.
Nature. 2018 Sep;561(7722):263-267. doi: 10.1038/s41586-018-0475-6. Epub 2018 Sep 12. - Malinverno C, Corallino S, Giavazzi F, Bergert M, Li Q, Leoni M, Disanza A, Frittoli E, Oldani A, Martini E, Lendenmann T, Deflorian G, Beznoussenko GV, Poulikakos D, Haur OK, Uroz M, Trepat X, Parazzoli D, Maiuri P, Yu W, Ferrari A, Cerbino R, Scita G.
Endocytic reawakening of motility in jammed epithelia.
Nat Mater. 2017 May;16(5):587-596. doi: 10.1038/nmat4848. Epub 2017 Jan 30. - Beznoussenko GV, Parashuraman S, Rizzo R, Polishchuk R, Martella O, Di Giandomenico D, Fusella A, Spaar A, Sallese M, Capestrano MG, Pavelka M, Vos MR, Rikers YG, Helms V, Mironov AA, Luini A.
Transport of soluble proteins the Golgi occurs by diffusion via continuities across cisternae.
Elife. 2014 May 27;3. doi: 10.7554/eLife.02009. - Kumar A, Mazzanti M, Mistrik M, Kosar M, Beznoussenko GV, Mironov AA, Garrè M, Parazzoli D, Shivashankar GV, Scita G, Bartek J, Foiani M.
ATR mediates a checkpoint at the nuclear envelope in response to mechanical stress.
Cell. 2014 Jul 31;158(3):633-46. doi: 10.1016/j.cell.2014.05.046. - Venditti R, Scanu T, Santoro M, Di Tullio G, Spaar A, Gaibisso R, Beznoussenko GV, Mironov AA, Mironov A Jr, Zelante L, Piemontese MR, Notarangelo A, Malhotra V, Vertel BM, Wilson C, De Matteis MA.
Sedlin controls the ER export of procollagen by regulating the Sar1 cycle.
Science. 2012 Sep 28;337(6102):1668-72. doi: 10.1126/science.1224947.
Methodological papers:
- Beznoussenko GV, and Mironov AA. Correlative video-light-electron microscopy of mobile organelles.
Methods Mol Biol. 2015; 1270: 321-46. doi: 10.1007/978-1-4939-2309-0_23. - Beznoussenko GV, Pilyugin SS, Geerts WJ, Kozlov MM, Burger KN, Luini A, Derganc J, Mironov AA.
Trans-membrane area asymmetry controls the shape of cellular organelles. Int J Mol Sci. 2015 Mar 9;16(3):5299-333. doi: 10.3390/ijms16035299. - Beznoussenko GV, Ragnini-Wilson A, Wilson C, Mironov AA.
Three-dimensional and immune electron microscopic analysis of the secretory pathway in Saccharomyces cerevisiae. Histochem Cell Biol. 2016 Nov;146(5):515-527. Epub 2016 Sep 3. - Mironov AA. Beznoussenko GV, Algorithm for Modern Electron Microscopic Examination of the Golgi Complex.
Methods Mol Biol. 2023;2557: 161-209. doi: 10.1007/978-1-0716-2639-9_12.PMID: 36512216 Review.
Photogallery
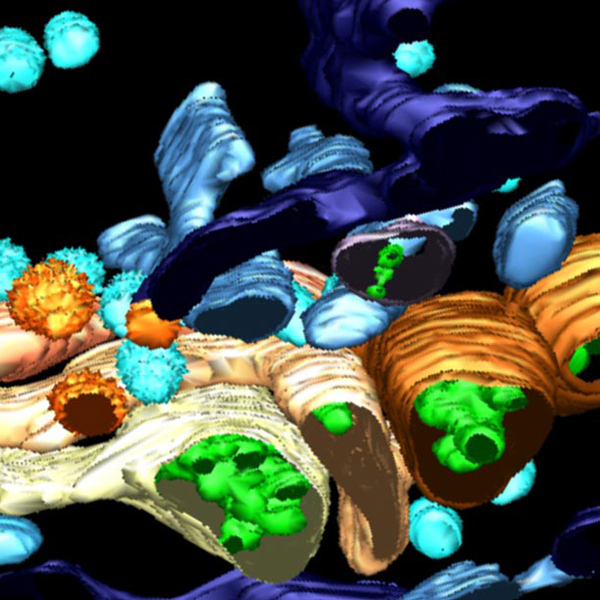
 3D reconstruction of Golgi apparatus
3D reconstruction of Golgi apparatus 3D reconstruction of Golgi apparatus
3D reconstruction of Golgi apparatus 3D reconstruction of Golgi apparatus
3D reconstruction of Golgi apparatusElectron Microscopy Instruments

Galina Beznusenko
Galina Beznusenko è responsabile della Core Facility di microscopia elettronica per cellule e tessuti presso l'IFOM, dove ricopre un ruolo chiave dal 2010. Si è laureata in Medicina e si è specializzata in Ostetricia e Ginecologia (1994, Istituto medico statale di Ivanovo, Russia) e Morfologia patologica (1996, Accademia medica di formazione post-laurea, San Pietroburgo, Russia). Galina ha poi conseguito un dottorato di ricerca presso l'Università Nazionale Russa di Ricerca Medica Pirogov, concentrandosi su ostetricia e ginecologia, istologia ed embriologia.
Nel 2007 ha conseguito il titolo di Dottore in Scienze presso la stessa università, specializzandosi in Istologia e Biologia Cellulare. Galina ha anche ricoperto ruoli di leadership, tra cui quello di Capo del Dipartimento di Patologia presso il Centro Medico di Oncologia di Vladimir per 5 anni.
Nel 1997, Galina Beznusenko si è trasferita in Italia, dove ha lavorato per 13 anni presso il Consorzio Mario Negri Sud. Nel 2010, insieme ad Alexandre Mironov, ha fondato il Laboratorio di Microscopia Elettronica e l'EM Core Facility presso l'IFOM, dove hanno costruito una struttura completamente nuova e all'avanguardia che supporta la ricerca di punta in vari ambiti scientifici.