Citofluorimetria

Panoramica
La citometria a flusso è una tecnologia avanzata per l’analisi e la separazione delle cellule in base alle loro caratteristiche fisiche e molecolari, fornendo informazioni preziose sia per la ricerca che per applicazioni cliniche. Dallo sviluppo negli anni ’60, è diventata uno strumento essenziale nella ricerca scientifica, grazie alla capacità di acquisire rapidamente dati, alla versatilità di applicazioni e alla possibilità di esplorare sistemi biologici complessi.
Negli ultimi anni, la citometria a flusso ha conosciuto progressi esponenziali. Mentre i primi strumenti potevano analizzare solo un numero limitato di parametri, i miglioramenti tecnologici progressivi ne hanno ampliato significativamente le capacità. L’introduzione della tecnologia full-spectrum ha rappresentato una svolta, consentendo l’analisi simultanea di oltre 50 parametri, come dimostrato da studi pubblicati.
Oltre al suo potere analitico, la citometria a flusso svolge un ruolo cruciale in immunologia, dove la capacità di identificare e separare popolazioni cellulari specifiche è indispensabile. Più in generale, continua a stimolare scoperte sulla funzione cellulare, sui meccanismi delle malattie e sullo sviluppo di terapie.
Il Flow Cytometry Core Facility presso IFOM mette a disposizione tecnologie all’avanguardia e strumentazione di ultima generazione, gestite da un team altamente esperto con decenni di esperienza. La struttura supporta una vasta gamma di applicazioni, tra cui immunofenotipizzazione, analisi del ciclo cellulare, studi sul metabolismo, saggi di apoptosi e proliferazione cellulare, analisi di proteine fluorescenti e rilevazione di citochine, chemochine e proteine intra/extra-cellulari.
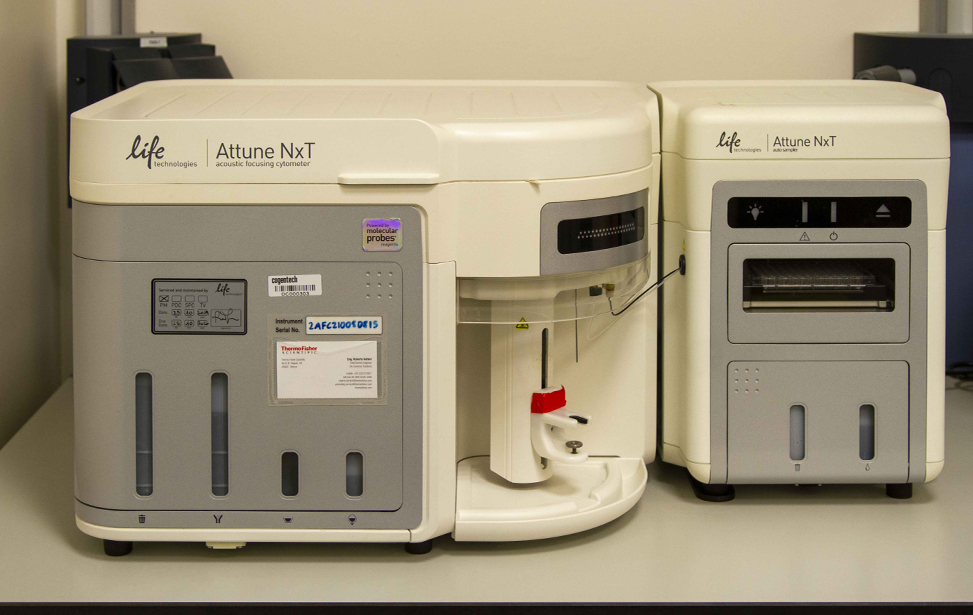
Gli utenti hanno accesso sia a citometri tradizionali (FACSCanto II, Attune NxT) sia a strumenti spettrali avanzati (Aurora 5L). L’uso indipendente di questi strumenti è consentito solo al termine di un corso teorico-pratico organizzato dal personale della facility.
Per la separazione cellulare (cell sorting), l’accesso è disponibile solo con assistenza. La facility offre sia sorter convenzionali (MoFlo Astrios, FACSAria IIU) sia un sorter spettrale (Aurora CS).
Inoltre, la struttura collabora con il team di bioinformatica per fornire servizi di analisi dati ad alto numero di parametri. Il personale esperto è disponibile per fornire supporto e consulenza durante l’intero processo sperimentale, inclusi design dei pannelli, ottimizzazione e risoluzione dei problemi.
Il Flow Cytometry Core Facility garantisce l’ottimale configurazione, manutenzione e prestazioni degli strumenti. Il personale della facility fornisce consulenza esperta sulla preparazione dei campioni, sul design dei pannelli e sulle strategie di gating.
Analisi dei dati & software
- Kaluza
- FlowJo
- FCS Express
- SpectroFlo
- FACSDiva
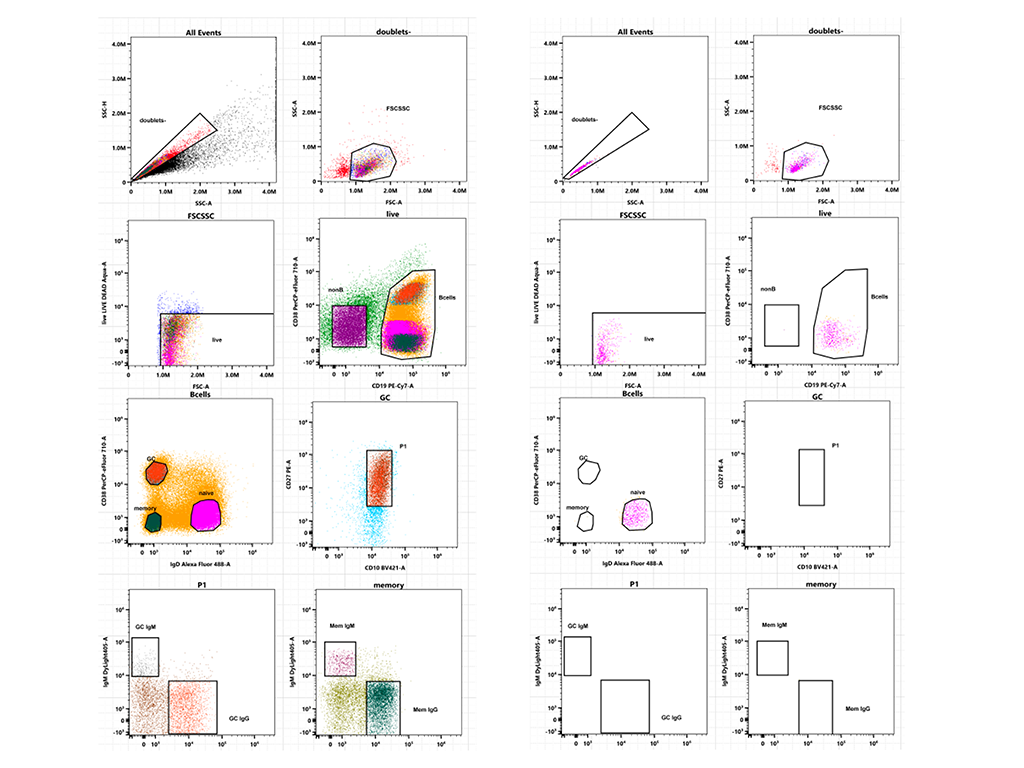
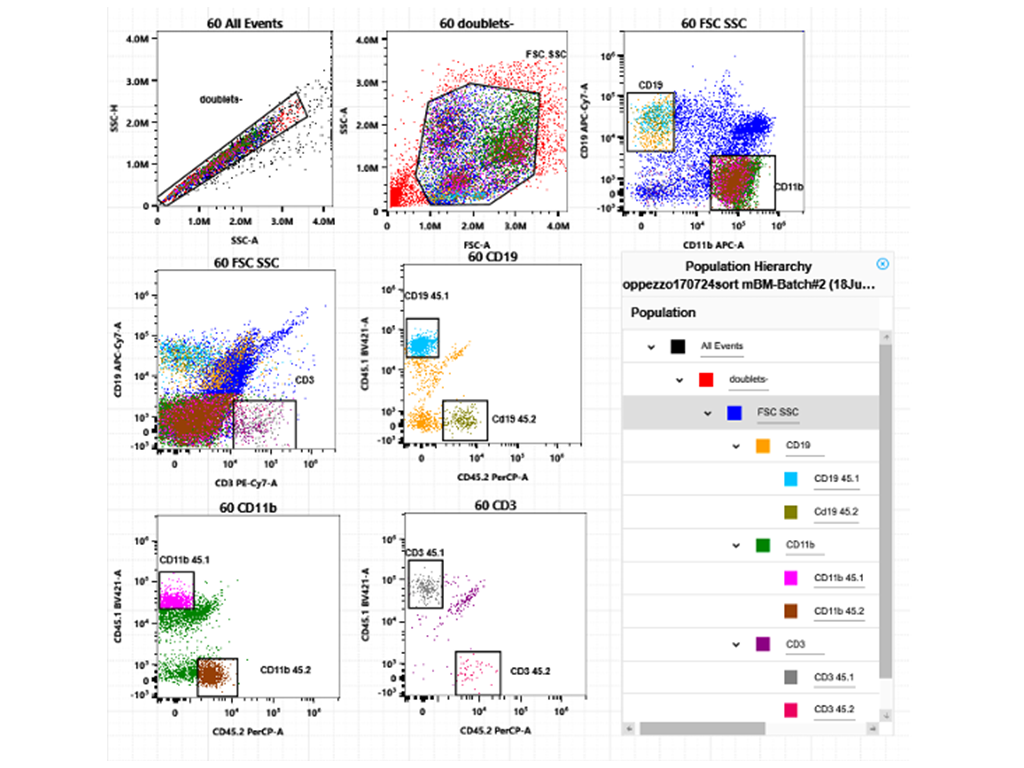
Identificazione delle sottopopolazioni cellulari
La facility è specializzata nell’identificazione di sottopopolazioni cellulari a partire da diversi campioni umani e murini, tessuti e colture 3D (sferoidi, organoidi, co-colture) mediante colorazioni multiparametriche. Queste includono:
- Subpopolazioni immunitarie (Treg, Tnaive, Tconv, GC Bcell, Bcell naive, TIL, TAM…)
- Cellule staminali tumorali (ALDH, Cd44/Cd24)
- Cellule endoteliali
- Cellule di mieloma
- Fibroblasti cardiaci
Analisi del ciclo cellulare e proliferazione
Saggi di citometria a flusso per l’analisi del ciclo cellulare e della proliferazione in cellule di mammifero e di lievito mediante:
- Propidium Iodine
- Sytox
- BrdU
- EdU
- FUCCI
- Cicline
- Ki67
Analisi del metabolismo cellulare:
- Assorbimento del glucosio (2NDBG)
- Visualizzazione dei lipidi (Bodipy) e delle lipid droplets (Nile Red)
- Funzionamento dei mitocondri (JC1, Mitotracker, Mitosox)
- Rilevamento di proteine intracellulari (TMR HaloTag)
- Rilevamento di specie reattive dell'ossigeno (CellRox, DFCDA)
- Monitoraggio del rapporto ATP/ADP (sensore Perceval)
Analisi della morte cellulare/apoptosi
- Caspase3
- AnnV\PI
- DRAQ7
Analisi delle proteine fluorescenti e del gene editing
- Analisi di linee cellulari transdotte, trasfettate o ingegnerizzate con CRISPR/Cas9 o cellule primarie (umane e murine)
- Detezione di proteine fluorescenti (GFP, RFP, mCherry, Scarlet, Tomato, YFP…)
- Lineage tracking con marcatura RGB barcoding
- Analisi dell'interazione proteica (kit Duolink flowPLA®
- Analisi dell'endocitosi cellulare (assorbimento di destrano)
- Analisi dell'assorbimento di microplastiche in diverse linee cellulari e in tessuti murini
- Quantificazione di antigen bound per cell (ABC) tramite QuantiBrite™ beads
Sorting
- Sorting bulk
- Sorting su supporti speciali per successive analisi (vetrini per imaging, piastre da 96 wells per screening/sequenziamento/spettrometria di massa/high content imaging)
- Sorting di singola cellula in piastre da 96 o 384 wells
- Sorting con precauzioni particolari per analisi metabolomiche/analisi NGS
Principali utilizzatori della facility (IFOM Research Groups):
Ringraziamenti alla Facility
In base alle Core Facilities Guidelines, qualora i servizi di una Facility siano stati utilizzati in un lavoro descritto in una pubblicazione, la Facility deve essere citata nei ringraziamenti, indicando sia il nome della Facility sia il relativo Research Resource Identifier (RRID).
Esempio di ringraziamento:
Il lavoro descritto è stato supportato dalla IFOM Citofluometria Core Facility (RRID: SCR_026865).
Co‑Authorship
Se un membro dello staff di una Core Facility IFOM o Cogentech contribuisce in modo sostanziale a un lavoro pubblicato, deve essere incluso come co‑autore.
Ulteriori informazioni sono disponibili nelle sezioni Recommended guidelines e Acknowledging and citing core facilities
Esempi di contributi sostanziali che possono giustificare la co‑autorship includono:
- Contributo alla progettazione sperimentale o all’ottimizzazione degli esperimenti
- Sviluppo o adattamento significativo di metodi o protocolli
- Analisi avanzata e interpretazione dei dati
- Contributo intellettuale che ha influenzato la direzione scientifica dello studio
Il supporto tecnico di routine o l’erogazione di servizi standard, di norma, giustificano il solo ringraziamento e non la co‑autorship.
- PMID: 37713487
Clonal cooperation through soluble metabolite exchange facilitates metastatic outgrowth by modulating Allee effect.
Hershey BJ, Barozzi S, Orsenigo F, Pompei S, Iannelli F, Kamrad S, Matafora V, Pisati F, Calabrese L, Fragale G, Salvadori G, Martini E, Totaro MG, Magni S, Guan R, Parazzoli D, Maiuri P, Bachi A, Patil KR, Cosentino Lagomarsino M, Havas KM. Sci Adv. 2023 Sep 15;9(37):eadh4184. doi: 10.1126/sciadv.adh4184. Epub 2023 Sep 15. Free PMC article. - PMID: 37108076
Short-Term Exposure to Benzo(a)Pyrene Causes Disruption of GnRH Network in Zebrafish Embryos.
Gentile I, Vezzoli V, Martone S, Totaro MG, Bonomi M, Persani L, Marelli F. Int J Mol Sci. 2023 Apr 7;24(8):6913. doi: 10.3390/ijms24086913. Free PMC article. - PMID: 35918044
HDAC6 inhibition decreases leukemic stem cell expansion driven by Hedgehog hyperactivation by restoring primary ciliogenesis.
Pezzotta A, Gentile I, Genovese D, Totaro MG, Battaglia C, Leung AY, Fumagalli M, Parma M, Cazzaniga G, Fazio G, Alcalay M, Marozzi A, Pistocchi A. Pharmacol Res. 2022 Sep;183:106378. doi: 10.1016/j.phrs.2022.106378. Epub 2022 Jul 30. - PMID: 33653693
CD4 T Cell-Dependent Rejection of Beta-2 Microglobulin Null Mismatch Repair-Deficient Tumors.
Germano G, Lu S, Rospo G, Lamba S, Rousseau B, Fanelli S, Stenech D, Le DT, Hays J, Totaro MG, Amodio V, Chilà R, Mondino A, Diaz LA Jr, Di Nicolantonio F, Bardelli A. Cancer Discov. 2021 Jul;11(7):1844-1859. doi: 10.1158/2159-8290.CD-20-0987. Epub 2021 Mar 2. - PMID: 33436662
MITO-Luc/GFP zebrafish model to assess spatial and temporal evolution of cell proliferation in vivo.
de Latouliere L, Manni I, Ferrari L, Pisati F, Totaro MG, Gurtner A, Marra E, Pacello L, Pozzoli O, Aurisicchio L, Capogrossi MC, Deflorian G, Piaggio G. Sci Rep. 2021 Jan 12;11(1):671. PMID: 33436662 Free PMC article. - PMID: 33015043
HDAC8: A Promising Therapeutic Target for Acute Myeloid Leukemia.
Spreafico M, Gruszka AM, Valli D, Mazzola M, Deflorian G, Quintè A, Totaro MG, Battaglia C, Alcalay M, Marozzi A, Pistocchi A. Front Cell Dev Biol. 2020 Sep 4;8:844. doi: 10.3389/fcell.2020.00844. eCollection 2020. PMID: 33015043 Free PMC article.
Pre IFOM Publications – Totaro
- PMID: 33903766
Heme catabolism by tumor-associated macrophages controls metastasis formation.
Consonni FM, Bleve A, Totaro MG, Storto M, Kunderfranco P, Termanini A, Pasqualini F, Alì C, Pandolfo C, Sgambelluri F, Grazia G, Santinami M, Maurichi A, Milione M, Erreni M, Doni A, Fabbri M, Gribaldo L, Rulli E, Soares MP, Torri V, Mortarini R, Anichini A, Sica A. Nat Immunol. 2021 May;22(5):595-606. doi: 10.1038/s41590-021-00921-5. Epub 2021 Apr 26. - PMID: 32265223
Tumor-Derived Prostaglandin E2 Promotes p50 NF-κB-Dependent Differentiation of Monocytic MDSCs.
Porta C, Consonni FM, Morlacchi S, Sangaletti S, Bleve A, Totaro MG, Larghi P, Rimoldi M, Tripodo C, Strauss L, Banfi S, Storto M, Pressiani T, Rimassa L, Tartari S, Ippolito A, Doni A, Soldà G, Duga S, Piccolo V, Ostuni R, Natoli G, Bronte V, Balzac F, Turco E, Hirsch E, Colombo MP, Sica A. Cancer Res. 2020 Jul 1;80(13):2874-2888. doi: 10.1158/0008-5472.CAN-19-2843. Epub 2020 Apr 7. - PMID: 18467122
Macrophage polarization in tumour progression.
Sica A, Larghi P, Mancino A, Rubino L, Porta C, Totaro MG, Rimoldi M, Biswas SK, Allavena P, Mantovani A. Semin Cancer Biol. 2008 Oct;18(5):349-55. doi: 10.1016/j.semcancer.2008.03.004. Epub 2008 Mar 26. Review. - PMID: 21995571
Macrophages in cancer and infectious diseases: the 'good' and the 'bad'.
Porta C, Riboldi E, Totaro MG, Strauss L, Sica A, Mantovani A. Immunotherapy. 2011 Oct;3(10):1185-202. doi: 10.2217/imt.11.116. Review. - PMID: 26267538
RORC1 Regulates Tumor-Promoting "Emergency" Granulo-Monocytopoiesis.
Sica A, Larghi P, Mancino A, Rubino L, Porta C, Totaro MG, Rimoldi M, Biswas SK, Allavena P, Mantovani A. Semin Cancer Biol. 2008 Oct;18(5):349-55. doi: 10.1016/j.semcancer.2008.03.004. Epub 2008 Mar 26. Review. - PMID:19616341
Cellular and molecular pathways linking inflammation and cancer.
Porta C, Larghi P, Rimoldi M, Totaro MG, Allavena P, Mantovani A, Sica A. Immunobiology. 2009;214(9-10):761-77. doi: 10.1016/j.imbio.2009.06.014. Epub 2009 Jul 17. Review. - PMID: 21948460
Origin and Functions of Tumor-Associated Myeloid Cells (TAMCs).
Sica A, Porta C, Morlacchi S, Banfi S, Strauss L, Rimoldi M, Totaro MG, Riboldi E. Cancer Microenviron. 2012 Aug;5(2):133-49. doi: 10.1007/s12307-011-0091-6. Epub 2011 Sep 24. Free PMC article. - PMID: 23049782
The p50 subunit of NF-κB orchestrates dendritic cell lifespan and activation of adaptive immunity.
Larghi P, Porta C, Riboldi E, Totaro MG, Carraro L, Orabona C, Sica A. PLoS One. 2012;7(9):e45279. doi: 10.1371/journal.pone.0045279. Epub 2012 Sep 25. Free PMC article. - PMID: 17825402
The histone H3 lysine-27 demethylase Jmjd3 links inflammation to inhibition of polycomb-mediated gene silencing.
De Santa F, Totaro MG, Prosperini E, Notarbartolo S, Testa G, Natoli G. Cell. 2007 Sep 21;130(6):1083-94. doi: 10.1016/j.cell.2007.08.019. Epub 2007 Sep 6. Free article. - PMID: 22127978
Enhanced interferon regulatory factor 3 binding to the interleukin-23p19 promoter correlates with enhanced interleukin-23 expression in systemic lupus erythematosus.
Smith S, Gabhann JN, Higgs R, Stacey K, Wahren-Herlenius M, Espinosa A, Totaro MG, Sica A, Ball E, Bell A, Johnston J, Browne P, O'Neill L, Kearns G, Jefferies CA. Arthritis Rheum. 2012 May;64(5):1601-9. doi: 10.1002/art.33494. Free article. - PMID: 18716661
The histone H3 lysine 27-specific demethylase Jmjd3 is required for neural commitment.
Burgold T, Spreafico F, De Santa F, Totaro MG, Prosperini E, Natoli G, Testa G. PLoS One. 2008 Aug 21;3(8):e3034. doi: 10.1371/journal.pone.0003034. Free PMC article.
Gallery Flow Cytometry unit
Strumentazione

Maria Grazia Totaro
Maria Grazia ha conseguito la laurea magistrale in Biologia applicata alla ricerca biomedica presso l’Università dell’Insubria a Varese. La sua formazione si è arricchita grazie a esperienze in istituti di ricerca di eccellenza come l’Istituto di Ricerca in Biomedicina (IRB) di Bellinzona e l’Istituto Europeo di Oncologia (IEO) e l’Istituto Humanitas di Milano, dove ha collaborato con ricercatori di spicco nel campo dell’immunologia.
Durante il suo dottorato presso l’Istituto Humanitas, l’interesse per l’immunologia l’ha condotta a scoprire il mondo della citofluorimetria, rivelandone le straordinarie potenzialità.
Conseguito il PhD, ha messo a frutto le competenze acquisite entrando a far parte dell’unità di Imaging di IFOM, sotto la guida del Dr. Dario Parazzoli, come tecnico specializzato in citofluorimetria. Nel corso di 10 anni, Maria Grazia ha consolidato le sue competenze e fornito un contributo significativo alla crescita e allo sviluppo delle attività di citofluorimetria dell’unità, diventandone un punto di riferimento.
A ottobre 2024, è stata nominata Head of Facility dell’unità di Citofluorimetria, istituita a seguito della divisione dell’unità di Imaging, assumendo la responsabilità di guidare questa nuova realtà verso l’eccellenza scientifica.