Risposta al danno al DNA e senescenza cellulare
Introduzione
Risposta al danno al DNA e senescenza cellulare è un programma di ricerca IFOM coordinato da Fabrizio d'Adda di Fagagna e dedicato allo studio dell'invecchiamento cellulare come barriera contro il cancro.
La vita della cellula non è immortale. Solo le cellule tumorali conquistano l'immortalità proliferando senza controllo a scapito dell'intero organismo.
Per le cellule normali, invece, esiste un limite alla proliferazione, a cui negli anni '60 del secolo scorso fu dato il nome di limite di Hayflick, dal biologo cellulare che per primo lo osservò.
In sostanza, il limite di Hayflick sta a indicare l'esistenza di una fase in cui, con l'avvio di un processo noto come senescenza cellulare, si arresta permanentemente ogni evento proliferativo della cellula.
Si tratta di una forma di senescenza a livello cellulare che è alla base dell'invecchiamento dell'intero organismo, un meccanismo che l'evoluzione ha selezionato come arma contro lo sviluppo di tumori, proprio per la sua capacità intrinseca di bloccare la crescita delle cellule.
Quando, infatti, viene accidentalmente alterato e conseguentemente iperattivato uno di quei geni capaci di stimolare la proliferazione cellulare - i cosiddetti oncogeni, veri e propri acceleratori della trasformazione maligna - per tutta risposta la cellula mette in atto contromisure anti-proliferative scatenando proprio il programma di senescenza cellulare.
Cosa innesca questo processo durante l'invecchiamento o quando la cellula è a rischio cancro?
Per rispondere a questa e a molte altre domande che ruotano attorno a questo aspetto della biologia dei tumori, IFOM ha deciso di sviluppare il programma Risposta al danno al DNA e senescenza cellulare, nell'ambito del quale Fabrizio d'Adda di Fagagna e il team di scienziati che coordina sono impegnati a studiare i dettagli molecolari del processo di senescenza e gli eventi che vedono protagonisti i telomeri, ovvero le regioni di protezione all'estremità dei cromosomi, dove rimangono i segni delle avvenute divisioni cellulari e dove rimane traccia del tempo che passa e dei danni che il patrimonio genetico può subire nel corso della vita di una cellula. Lo scopo ultimo di queste ricerche è:
decifrare i segnali molecolari che attivano il processo di senescenza cellulare e le sue dinamiche;
comprendere il ruolo dei telomeri nell'invecchiamento e nel cancro;
capire in che modo la senescenza cellulare blocca lo sviluppo tumorale.
L'ambito biologico
Il programma di ricerca IFOM Risposta al danno al DNA e senescenza cellulare studia i sistemi che la cellula ha a disposizione per controllare e bloccare la propria proliferazione, al fine di capire in che modo questi vengano impiegati per fermare la progressione tumorale.
Le cellule, in condizioni normali, hanno una limitata capacità di espansione: sono programmate per moltiplicarsi al fine di costruire e mantenere organi e tessuti, ma poi esauriscono il proprio potenziale proliferativo.
Allora smettono di rispondere alla miriade di segnali che prima ne stimolavano la crescita, si arrestano in modo permanente e vanno incontro a cambiamenti morfologici e molecolari caratteristici.
Un comportamento simile, però, possono sorprendentemente averlo anche le cellule tumorali, all'inizio della loro trasformazione.
È quello che viene riscontrato, per esempio, in cellule normali costrette sperimentalmente a esprimere in modo anomalo un oncogene. Ed è anche ciò che si osserva nelle cellule di molte lesioni tumorali prima che diventino aggressive e maligne.
La senescenza cellulare, in questi casi, funziona da sistema di difesa per arginare la progressione dei tumori, impedendo la moltiplicazione delle cellule.
Che sia senescenza legata all'invecchiamento o evocata all'insorgere di un cancro, la scintilla che innesca l'entrata di una cellula in questo stato di arresto permanente di ogni attività proliferativa è fondamentalmente la stessa: la presenza nel DNA di danni irrisolvibili e l'attivazione del DDR (dall'inglese DNA Damage Response), il complesso meccanismo molecolare di risposta a essi.
A ogni divisione cellulare il genoma subisce in maniera del tutto fisiologica un particolarissimo danno: le punte estreme dei suoi cromosomi - i telomeri privi di geni - perdono pezzi per l'incapacità dei sistemi di copiatura del DNA di portare a termine le operazioni a livello di queste speciali regioni.
È questo accorciamento progressivo dei telomeri che porta una cellula normale, con il trascorrere del tempo a smettere di proliferare.
Consumato il DNA telomerico - che in pratica protegge dall'erosione il resto del materiale genetico ricco di geni - l'inesorabile processo finirebbe col mettere in pericolo l'integrità del genoma.
Se ciò accadesse sarebbe la catastrofe, ma non accade perché - e questo si sa proprio grazie al contributo di d'Adda di Fagagna - quando si arriva a questo punto di non ritorno scatta un allarme persistente, si attiva il DDR, che a sua volta porta la cellula alla senescenza.
Sempre i telomeri, oltre a essere smangiati dal tempo, sono anche potenziali punti di accumulo di danni al DNA e fonti di allarmi continui perché, a differenza del resto del genoma, sono irreparabili in caso di rottura.
E ancora i telomeri in modo particolare, ma anche tutto il resto del genoma, vengono stressati al punto da richiamare il DDR e con esso il programma di senescenza, quando la cellula viene iper-stimolata a proliferare e duplicare il proprio materiale genetico, come succede all'inizio della trasformazione tumorale, qualora venga alterato un oncogene.
Gli obiettivi del programma
Telomeri, senescenza, DDR, cancro: le scoperte degli ultimi decenni li mettono sempre più a fuoco come facce e spigoli differenti dello stesso complicato poliedro.
Per questo motivo il principale obiettivo dell'unità diretta da Fabrizio d'Adda di Fagagna è capire come sono intimamente connessi e in che relazione sono tra loro.
Ciò in pratica significa studiare a fondo il fenomeno della senescenza cellulare e il DDR e individuarne tutti gli attori molecolari, comprendere il ruolo dei telomeri e investigare i diversi eventi di cui questi sono protagonisti.
Accanto a questo, poi, capire cosa accade all'interno di una cellula quando viene iper-attivato un oncogene, quali forze molecolari un evento del genere scatena e come funziona in questo contesto la barriera della senescenza.
Gli approcci
Aspetti sperimentali cruciali per comprendere la senescenza cellulare sono l'identificazione e la visualizzazione, all'interno del patrimonio genetico nucleare, di tutte le regioni da cui partono segnali molecolari persistenti capaci di innescare il processo.
Per fare questo, il team diretto da d'Adda di Fagagna si avvale di avanzate tecnologie per lo studio in microscopia ottica, come la microscopia a fluorescenza e microscopia confocale, grazie alla quale cattura immagini caratteristiche delle cellule e del patrimonio genetico all'interno di esse.
Tecnologie di sequenziamento all'avanguardia e sofisticati sistemi di silenziamento dei geni, inoltre, permettono a quest'unità di analizzare, nel dettaglio della sequenza, il genoma e tutti i suoi prodotti di trascrizione durante l'intero arco di vita delle cellule, in particolare nel momento in cui si innesca la senescenza, e di andare a caccia dei determinanti molecolari del processo, siano essi DNA, RNA o proteine.
Impatto su diagnosi, prevenzione o trattamento dei tumori
Studiare la senescenza cellulare e il suo ruolo nell'invecchiamento e nel cancro, la vulnerabilità dei telomeri e gli stress che violano l'integrità del genoma fornisce strumenti non solo per capire le dinamiche dell'insorgenza e della progressione dei tumori.
Molti farmaci chemioterapici convenzionali generano danni al DNA e in alcuni casi potrebbero non uccidere le cellule tumorali ma indurne la senescenza. Capire i determinanti di questo processo, quindi, ha forti implicazioni per la comprensione degli effetti di queste terapie.
La biologia dei telomeri che sta emergendo da questi studi, poi, fornisce un forte razionale biologico per l'impiego di particolari strategie terapeutiche che sono oggi al vaglio della sperimentazione clinica.
Bloccare a un certo punto l'erosione delle estremità cromosomiche causata dagli eventi di proliferazione è una necessità che non caratterizza solo le cellule normali.
Anche quelle tumorali, infatti, sono costrette a farlo per non polverizzare il proprio materiale genetico.
Mentre le cellule sane ricorrono alla senescenza, quelle tumorali impiegano un sistema diverso: attivano la telomerasi, uno speciale enzima che mantiene intatto il DNA telomerico e ne previene gli stress e contro il quale sono stati sviluppati diversi approcci terapeutici.
Considerato il ruolo dei telomeri nel cancro, la telomerasi, assente nella maggior parte delle cellule dell'organismo ed espressa nell'80% di quelle tumorali, rappresenta teoricamente un bersaglio ideale per arrivare a colpire le cellule malate lasciando intatte quelle sane.
 d'Adda di Fagagna Lab
Ricercatore
Pubblicazioni
Stampa&Media
Membri del gruppo
Contatta il ricercatore
d'Adda di Fagagna Lab
Ricercatore
Pubblicazioni
Stampa&Media
Membri del gruppo
Contatta il ricercatorePhotogallery
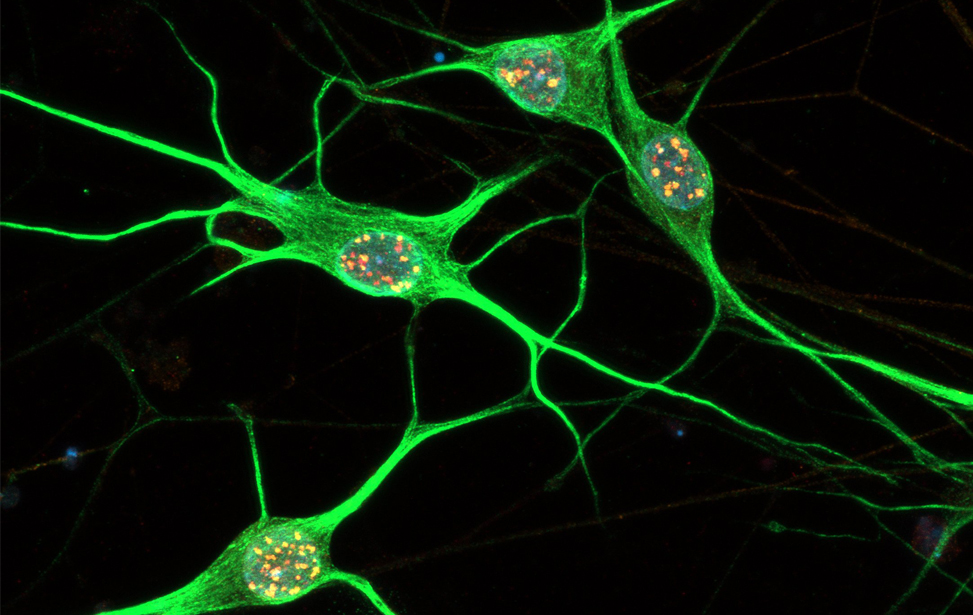 Immunostaining of human motor neurons upon IR treatment (2Gy). Merge signal of MAP2 (green), DAPI (blue), γH2AX (red) and pATM (magenta)
Immunostaining of human motor neurons upon IR treatment (2Gy). Merge signal of MAP2 (green), DAPI (blue), γH2AX (red) and pATM (magenta)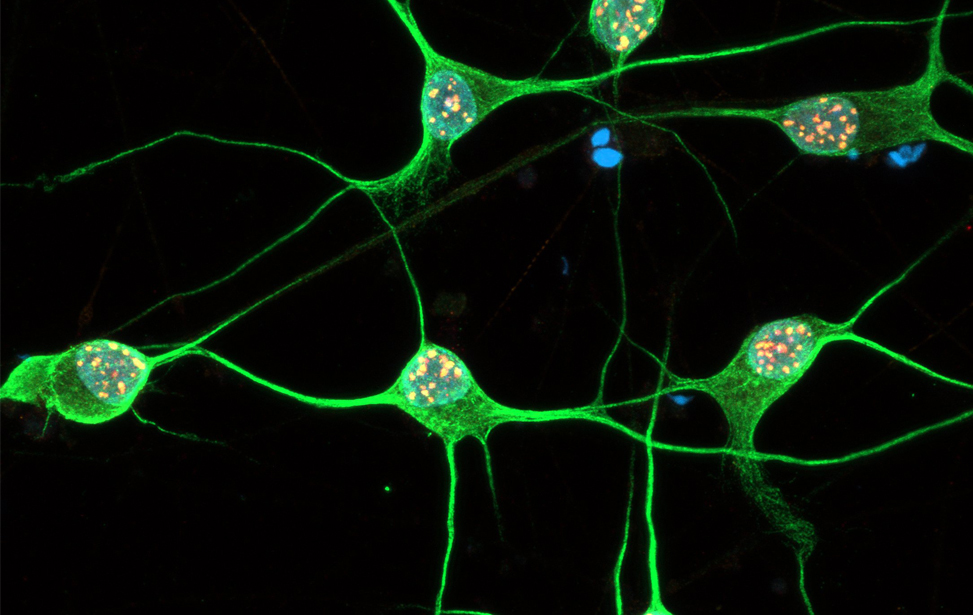 Immunostaining of human motor neurons upon IR treatment (2Gy). Merge signal of MAP2 (green), DAPI (blue), γH2AX (red) and pATM (magenta)
Immunostaining of human motor neurons upon IR treatment (2Gy). Merge signal of MAP2 (green), DAPI (blue), γH2AX (red) and pATM (magenta)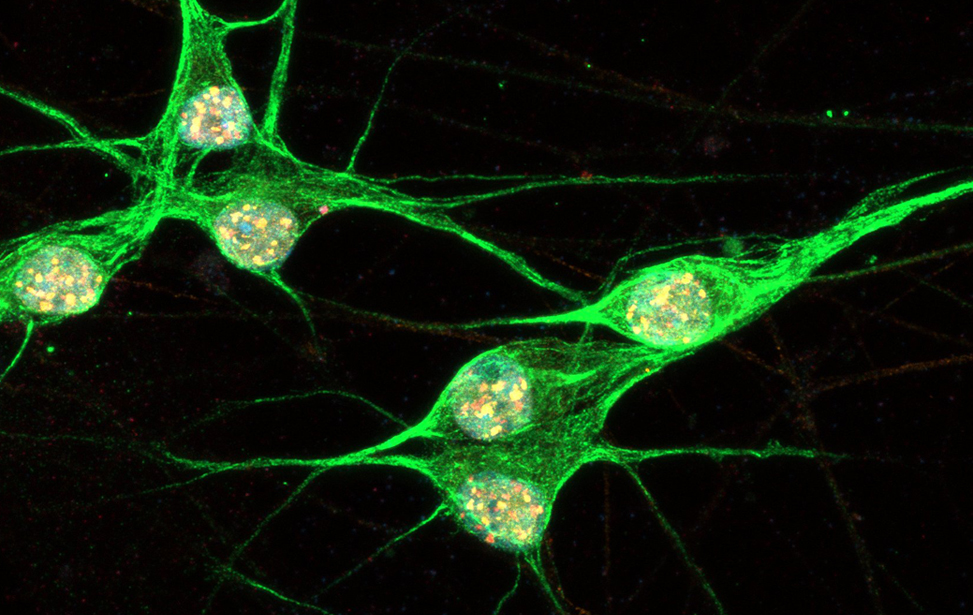 Immunostaining of human motor neurons upon IR treatment (2Gy). Merge signal of MAP2 (green), DAPI (blue), γH2AX (red) and pATM (magenta)
Immunostaining of human motor neurons upon IR treatment (2Gy). Merge signal of MAP2 (green), DAPI (blue), γH2AX (red) and pATM (magenta)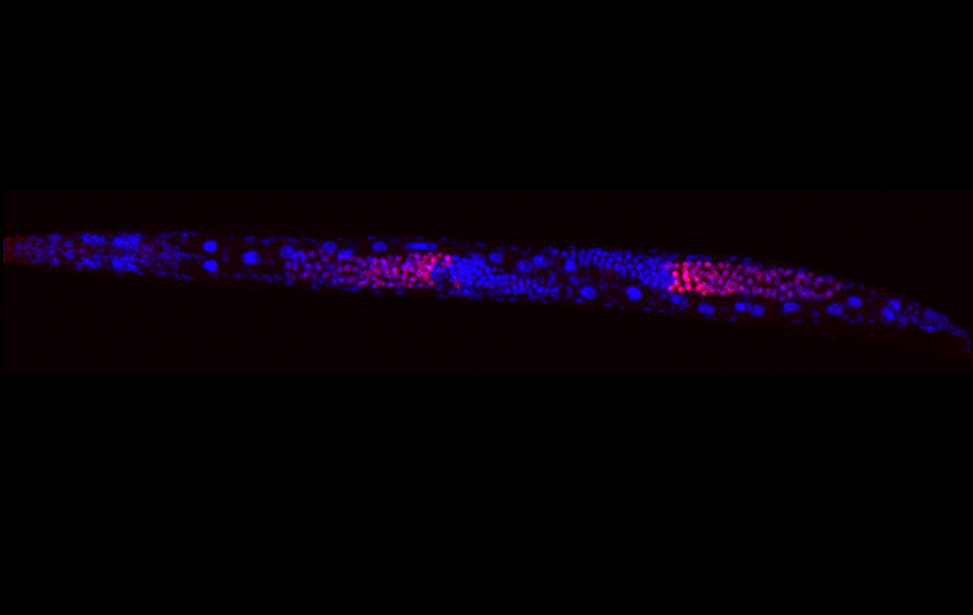 worm stq
worm stq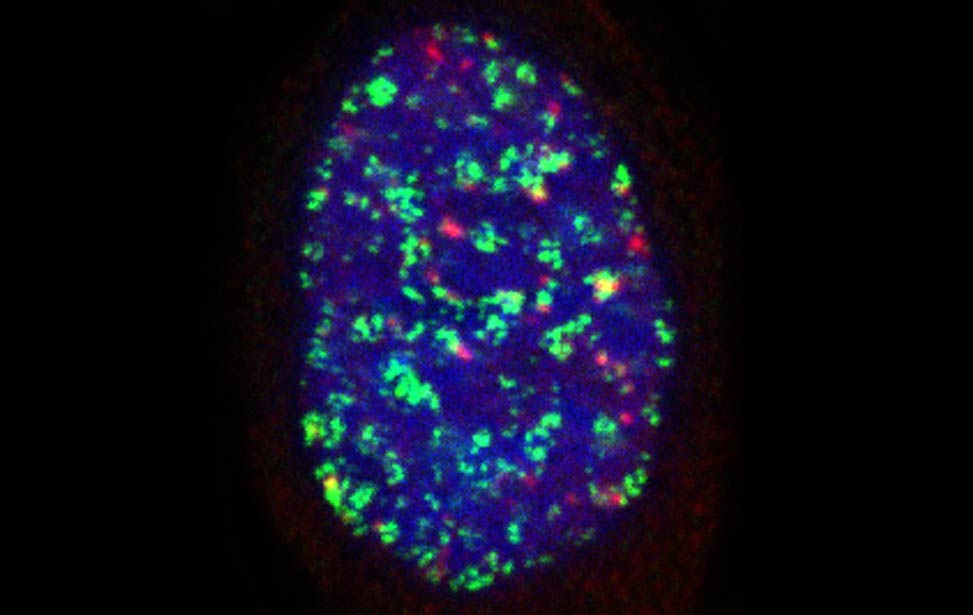 greenPCNA_red53BP1_rasD3
greenPCNA_red53BP1_rasD3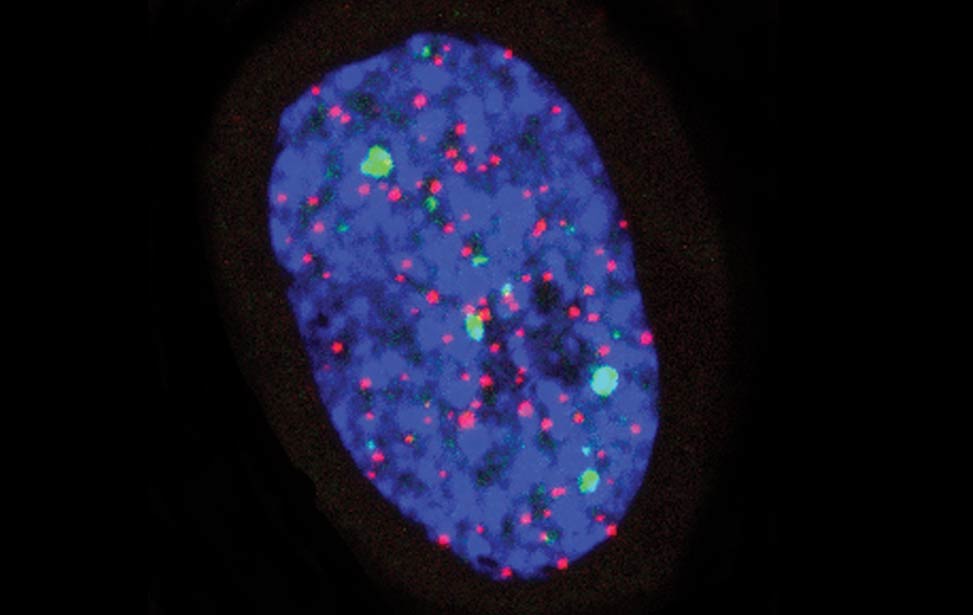 Fra - Senescent BJ DDR Telomeres
Fra - Senescent BJ DDR Telomeres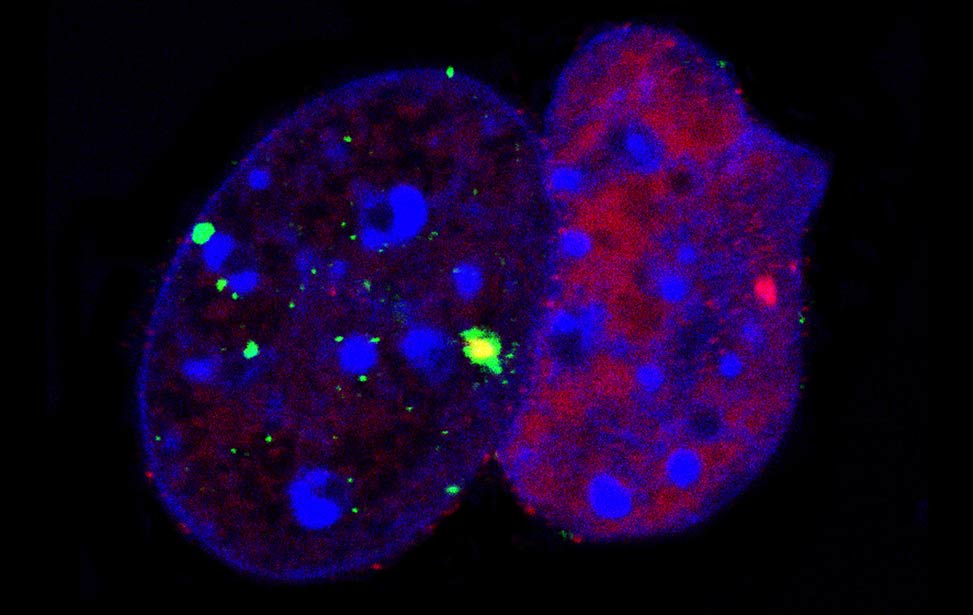 FLA_NIH24
FLA_NIH24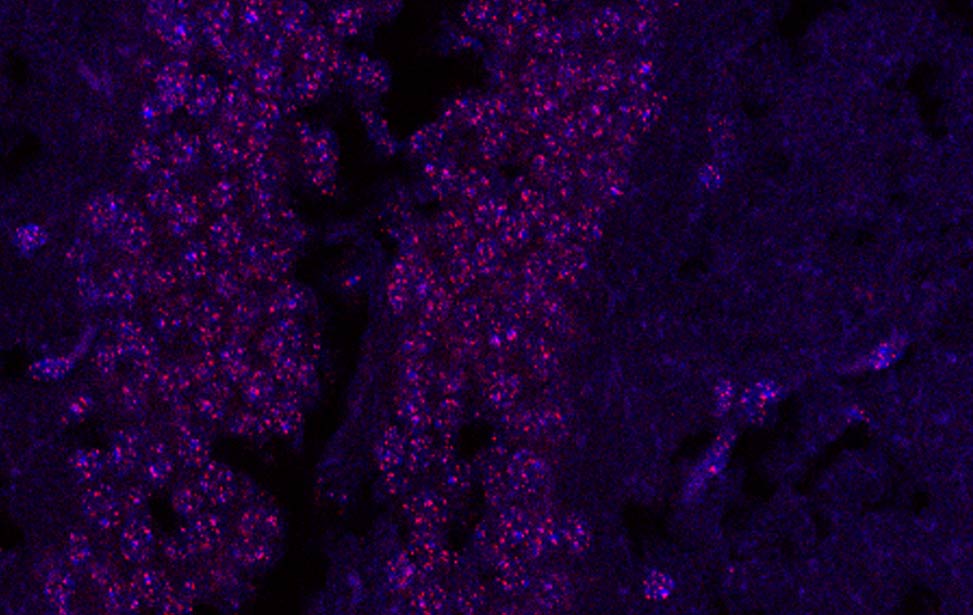 Fra - Mouse brain telomeres
Fra - Mouse brain telomeres